题目内容
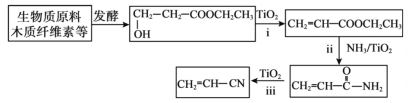
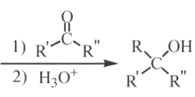
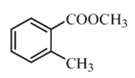
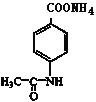
【题目】有机物甲的结构简式为:![]() ,它可以通过下列路线合成(分离方法和其他产物已经略去)
,它可以通过下列路线合成(分离方法和其他产物已经略去)

(1)写出 反应银氨溶液反应的化学方程式_____。
反应银氨溶液反应的化学方程式_____。
(2)写出甲发生聚合反应的化学方程式_____。
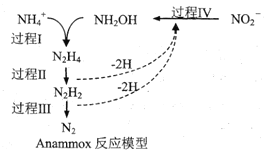
(3)步骤 I 和 IV 在合成甲过程中的目的是_____。
【答案】 + 2Ag(NH3)2OH
+ 2Ag(NH3)2OH![]()
 + 2Ag↓+3NH3 + H2O
+ 2Ag↓+3NH3 + H2O  +(n-1)H2O 保护氨基不被氧化(或保护氨基,防止氨基被氧化)
+(n-1)H2O 保护氨基不被氧化(或保护氨基,防止氨基被氧化)
【解析】
(1) 中醛基与银氨溶液反应生成-COONH4、Ag、氨气、水;
中醛基与银氨溶液反应生成-COONH4、Ag、氨气、水;
(2)![]() 通过生成肽键发生缩聚反应;
通过生成肽键发生缩聚反应;
(3)步骤Ⅰ是氨基生成肽键,步骤Ⅳ是肽键发生水解,重新生成氨基;
(1) 中醛基发生银镜反应,反应方程式是
中醛基发生银镜反应,反应方程式是 + 2Ag(NH3)2OH
+ 2Ag(NH3)2OH![]()
 + 2Ag↓+3NH3 + H2O;
+ 2Ag↓+3NH3 + H2O;
(2)![]() 通过生成肽键发生缩聚反应,反应方程式是
通过生成肽键发生缩聚反应,反应方程式是 +(n-1)H2O;
+(n-1)H2O;
(3)步骤Ⅰ是氨基生成肽键,步骤Ⅳ是肽键发生水解,重新生成氨基,步骤 I 和 IV 在合成甲过程中的目的是把—NH2暂时保护起来,防止在步骤Ⅲ中被氧化。

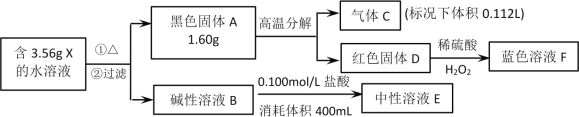
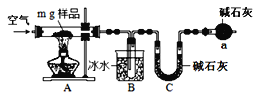
【题目】NaNO2是常用的一种防腐剂,其中+3价的N具有一定的氧化性。某实验小组利用以下反应2NO2+2NaOH=NaNO3+NaNO2+H2O制备NaNO2,并探究其性质。
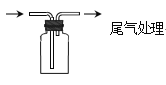
I.制备NaNO2
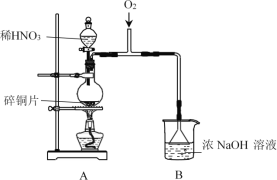
(1)A中发生反应的化学方程式是______。
(2)B中选用漏斗替代长直导管的优点是______。
(3)为检验B中制得NaNO2,甲进行以下实验:
序号 | 试管 | 操作 | 现象 |
① | 2mLB中溶液 | 加2mL0.1mol/LKI溶液,滴加几滴淀粉溶液 | 不变蓝 |
② | 2mLB中溶液 | 滴加几滴H2SO4至pH=5,加2mL0.1mol/LKI溶液,滴加几滴淀粉溶液 | 变蓝 |
③ | 2mLH2O | 滴加几滴H2SO4至pH=5,加2mL0.1mol/LKI溶液,滴加几滴淀粉溶液 | 不变蓝 |
实验③的目的是_______。
(4)乙认为上述3组实验无法证明B中一定含NaNO2,还需补充实验,理由是______。
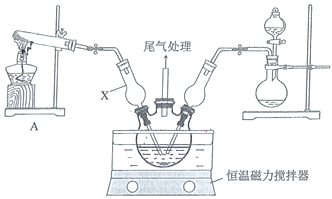
II.探究NaNO2的性质
装置 | 操作 | 现象 |
| 取10mL1mol/LNaNO2溶液于试剂瓶中,加入几滴H2SO4酸化,再加入10mL1mol·L-1FeSO4溶液,迅速塞上橡胶塞,缓缓通入足量O2。 | i.溶液迅速变为棕色; ii.溶液逐渐变浅,有无色气泡产生,溶液上方为浅红棕色。 iii.最终形成棕褐色溶液。 |
资料:i.
ii.HNO2在溶液中不稳定,易分解产生NO和NO2气体。
(5)现象i溶液变为棕色的原因是______。
(6)已知现象ii棕色溶液变浅是由于生成了Fe3+,反应的离子方程式是______。