题目内容
【题目】近年来我国科学家在青蒿素应用领城取得重大进展,如利用下述反应过程可以制取治疗疟疾的首选药青蒿琥酯。下列有关说法正确的是
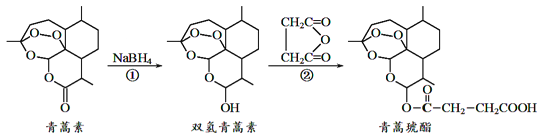
A. 青蒿素分子中所有碳原子在同一平面内
B. 反应①属于还原反应,反应②理论上原子利用率可达100%
C. 双氢青蒿素属于芳香族化合物
D. 青蒿琥酯可以发生水解、酯化以及加聚反应
【答案】B
【解析】青蒿素分子中含有“![]() ”结构,所以不可能所有碳原子在同一平面内,故A错误;反应①为青蒿素中碳氧双键转化为醇羟基,是加氢反应,所以反应①属于还原反应,反应②理论上原子利用率可达100%,故B正确;双氢青蒿素不含苯环,不属于芳香族化合物,故C错误;青蒿琥酯含有酯基可以发生水解反应、含有羧基可以发生酯化反应、没有碳碳双键不能发生加聚反应,故D错误。
”结构,所以不可能所有碳原子在同一平面内,故A错误;反应①为青蒿素中碳氧双键转化为醇羟基,是加氢反应,所以反应①属于还原反应,反应②理论上原子利用率可达100%,故B正确;双氢青蒿素不含苯环,不属于芳香族化合物,故C错误;青蒿琥酯含有酯基可以发生水解反应、含有羧基可以发生酯化反应、没有碳碳双键不能发生加聚反应,故D错误。

 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案【题目】一些食物的近似pH值如下表:
食物 | 苹果 | 葡萄 | 牛奶 | 玉米粥 |
pH | 2.9-3.3 | 3.5-4.6 | 6.3-6.6 | 6.8-8.0 |
人的胃液中含有盐酸,对于胃酸过多的人,空腹时最宜食用的是
A. 苹果 B. 葡萄 C. 牛奶 D. 玉米粥
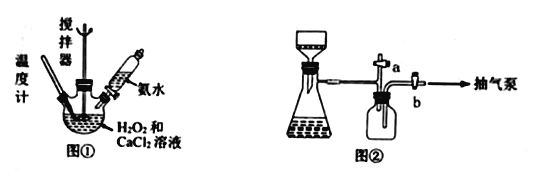
【题目】过氧化钙是一种在水产养殖中广泛使用的供氧剂。某实验研究小组用下图所示的装置制取过氧化钙并测定产品的含量。
有关过氧化钙的性质如下:
外观与性状 | 溶解性 | 稳定性 | |
过氧化钙(CaO2) | 白色结晶,无臭无味, 有潮解性 | 难溶于水,且不溶于 乙醇、乙醚 | 常温下稳定,加热至 315℃时开始分解 |
回答下列问题:
I.过氧化钙的制备
称取7.5gCaCl2·H2O,用5mL水溶解,加入25mL 30%的H2O2,边搅拌边滴加由5mL 浓NH3·H2O和20mL冷水配成的溶液,保持在0-5℃下充分反应半小时后抽滤,得到粗产品CaO2·8H2O。分别用少量冷水、乙醇洗涤该产品2~3次,在150℃下烘0.5-1h,冷却得到产品无水过氧化钙。
(1)图①盛装“CaCl2和H2O2混合液”的仪器名称______________________________。
(2)写出反应生成CaO2·8H2O的化学方程式___________________________________。
(3)抽滤后得到的晶体依次使用蒸馏水、乙醇洗涤,使用乙醇洗涤的目的是_________________________。
(4)用图②装置抽滤时,使用抽气泵抽真空前,应先关闭活塞____(填“a”或“b”)。
(5)反应温度以0~5℃为宜的原因____________________________。
II.产品中CaO2含量的测定
准确称取0.15g无水过氧化钙样品于锥形瓶中,加入50mL水和15mL2mol/LHCl,振荡使之溶解,立即用0.02mol/L的KMnO4溶液滴定至溶液呈微红色且半分钟内不褪色为止,重复实验3次,平均消耗20.00mL.KMnO4溶液。
(1)产品中CaO2的质量分数为_______________________________。
(2)若滴定后仰视读数,则测得样品中CaO2的含量___________(填“偏高”“偏低”或“不变”)