题目内容
右图是某同学设计的原电池装置,下列叙述中正确的是 ( )
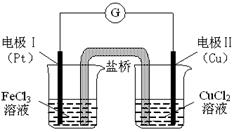

| A.电极Ⅰ上发生还原反应,作原电池的负极 |
| B.电极Ⅱ的电极反应式为:Cu2++2e-=Cu |
| C.该原电池的总反应为:2Fe3++Cu=Cu2++2Fe2+ |
| D.盐桥中装有含氯化钾的琼脂,其作用是传递电子 |
C
试题分析:A、铜的金属性强于Pt,因此Pt是正极,溶液中的铁离子得到电子发生还原反应,电极反应式为Fe3++e-=Fe2+,Pt是正极,A不正确;B、铜的金属性强于Pt,因此铜是负极,失去电子,电极反应式为Cu-2e-=Cu2+,B不正确;C、根据以上分析可知该原电池的总反应为:2Fe3++Cu=Cu2++2Fe2+,C正确;D、盐桥中装有含氯化钾的琼脂,其作用是传递阴阳离子,电子只能通过导线传递,D不正确,答案选C。

练习册系列答案
相关题目
 LaNi5H+NiOOH。下列有关说法不正确的是
LaNi5H+NiOOH。下列有关说法不正确的是 是某化学兴趣小组探究不同条件下化学能转变为电能的装置。请回答下列问题:
是某化学兴趣小组探究不同条件下化学能转变为电能的装置。请回答下列问题: 2Ni(OH)2,根据此反应式判断,此电池放电时,正极上发生反应的物质是( )。
2Ni(OH)2,根据此反应式判断,此电池放电时,正极上发生反应的物质是( )。