题目内容
为除去粗盐中的Ca2+、Mg2+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
称取粗盐
滤液
精盐
(1)步骤②中应加入的试剂是
(2)步骤④中应加入的试剂是
(3)若将第⑤步和第⑥步颠倒,会对实验结果产生影响,其原因是
称取粗盐
| ||
| ① |
| ② |
| ||
| ③ |
| ④ |
| ||
| ⑤ |
| ||
| ⑥ |
| ||
| ⑦ |
(1)步骤②中应加入的试剂是
BaCl2
BaCl2
溶液,判断此试剂已加过量的方法是取少量上层澄清液于试管中,滴加氯化钡溶液,不再产生白色沉淀,证明氯化钡溶液已滴加过量或取少量上层澄清液于试管中,滴加稀硫酸,产生白色沉淀,证明氯化钡溶液已滴加过量
取少量上层澄清液于试管中,滴加氯化钡溶液,不再产生白色沉淀,证明氯化钡溶液已滴加过量或取少量上层澄清液于试管中,滴加稀硫酸,产生白色沉淀,证明氯化钡溶液已滴加过量
.(2)步骤④中应加入的试剂是
Na2CO3
Na2CO3
溶液,第④步中相关的离子方程式是Ca2++CO32-═CaCO3↓、Ba2++CO32-═BaCO3↓
Ca2++CO32-═CaCO3↓、Ba2++CO32-═BaCO3↓
.(3)若将第⑤步和第⑥步颠倒,会对实验结果产生影响,其原因是
会使CaCO3、BaCO3、Mg(OH)2沉淀溶解,重新引入Ca2+、Ba2+、Mg2+
会使CaCO3、BaCO3、Mg(OH)2沉淀溶解,重新引入Ca2+、Ba2+、Mg2+
.分析:(1)根据加入氯化钡可以除去硫酸根离子进行解答;
(2)根据加入碳酸钠溶液能除去钙离子和剩余的钡离子进行解答;
(3)根据第⑤步和第⑥步颠倒会使CaCO3、BaCO3、Mg(OH)2沉淀溶解,重新引入Ca2+、Ba2+、Mg2+进行解答.
(2)根据加入碳酸钠溶液能除去钙离子和剩余的钡离子进行解答;
(3)根据第⑤步和第⑥步颠倒会使CaCO3、BaCO3、Mg(OH)2沉淀溶解,重新引入Ca2+、Ba2+、Mg2+进行解答.
解答:解:(1)加入氯化钡可以除去硫酸根离子,所以步骤②中应加入的试剂是氯化钡溶液,判断此试剂已加过量的方法是取少量上层澄清液于试管中,滴加氯化钡溶液,不再产生白色沉淀,证明氯化钡溶液已滴加过量或取少量上层澄清液于试管中,滴加稀硫酸,产生白色沉淀,证明氯化钡溶液已滴加过量,
故答案为:(1)BaCl2;取少量上层澄清液于试管中,滴加氯化钡溶液,不再产生白色沉淀,证明氯化钡溶液已滴加过量或取少量上层澄清液于试管中,滴加稀硫酸,产生白色沉淀,证明氯化钡溶液已滴加过量;
(2)加入碳酸钠溶液能除去钙离子和剩余的钡离子,相关的离子方程式是Ca2++CO32-═CaCO3↓、Ba2++CO32-═BaCO3↓,
故答案为:Na2CO3;Ca2++CO32-═CaCO3、Ba2++CO32-═BaCO3↓;
(3)第⑤步和第⑥步颠倒会使CaCO3、BaCO3、Mg(OH)2沉淀溶解,重新引入Ca2+、Ba2+、Mg2+,所以第⑤步和第⑥步不能颠倒,
故答案为:会使CaCO3、BaCO3、Mg(OH)2沉淀溶解,重新引入Ca2+、Ba2+、Mg2+.
故答案为:(1)BaCl2;取少量上层澄清液于试管中,滴加氯化钡溶液,不再产生白色沉淀,证明氯化钡溶液已滴加过量或取少量上层澄清液于试管中,滴加稀硫酸,产生白色沉淀,证明氯化钡溶液已滴加过量;
(2)加入碳酸钠溶液能除去钙离子和剩余的钡离子,相关的离子方程式是Ca2++CO32-═CaCO3↓、Ba2++CO32-═BaCO3↓,
故答案为:Na2CO3;Ca2++CO32-═CaCO3、Ba2++CO32-═BaCO3↓;
(3)第⑤步和第⑥步颠倒会使CaCO3、BaCO3、Mg(OH)2沉淀溶解,重新引入Ca2+、Ba2+、Mg2+,所以第⑤步和第⑥步不能颠倒,
故答案为:会使CaCO3、BaCO3、Mg(OH)2沉淀溶解,重新引入Ca2+、Ba2+、Mg2+.
点评:本题考查学生有关粗盐的提纯知识可以根据所学知识进行回答,难度不大.

练习册系列答案
相关题目


 为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):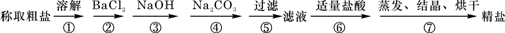

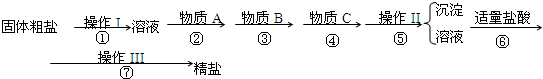
 aOH溶液 b、KOH溶液 c、BaCl2溶液 d、Ba(NO3)2溶液
aOH溶液 b、KOH溶液 c、BaCl2溶液 d、Ba(NO3)2溶液