题目内容
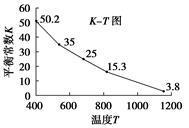
碘在水中溶解度很小,但易溶于KI溶液,因为发生反应:I2(aq)+I-(aq)=I3-。已知在不同温度下该反应的平衡常数如右图,下列说法不正确的是( )

A.上述反应正反应为放热反应
B.实验室配制碘水,为增大碘的溶解度可加入少量的KI
C.用该反应原理可除去硫粉中少量的碘单质
D.上述体系中加入苯,平衡不移动
【答案】
D
【解析】因温度越高,平衡常数越小,表明反应向右进行的程度减小,故正反应进行为放热反应,A对;由I2(aq)+I-(aq)=I3-知,B对;因硫不溶于KI而单质碘能溶,故将混合物投入KI溶液中即可除去碘单质,C对;加入苯后,碘被苯萃取,平衡发生移动,D错。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
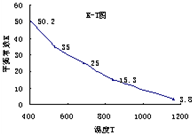 (2009?茂名二模)碘在水中溶解度很小,但易溶于KI溶液,因为发生反应:I2(aq)+I-(aq)=I3-.已知在不同温度下该反应的平衡常数如图,下列说法不正确的是( )
(2009?茂名二模)碘在水中溶解度很小,但易溶于KI溶液,因为发生反应:I2(aq)+I-(aq)=I3-.已知在不同温度下该反应的平衡常数如图,下列说法不正确的是( )