题目内容
在氧化还原反应中,电子转移的表示方法通常用单线桥法和双线桥法。试分析这两种表示方法的特征,并填空。
(1)标单线桥(4分)
KIO3+6HI=KI+3I2+3H2O氧化产物与还原产物物质的量之比= 。
(2)配平化学方程式及标双线桥(5分)
Fe + HNO3(稀)= Fe(NO3)2+ NO↑+ H2O反应中,氧化剂与还原剂的物质的量之比 。
(1)标单线桥(4分)
KIO3+6HI=KI+3I2+3H2O氧化产物与还原产物物质的量之比= 。
(2)配平化学方程式及标双线桥(5分)
Fe + HNO3(稀)= Fe(NO3)2+ NO↑+ H2O反应中,氧化剂与还原剂的物质的量之比 。
(1) 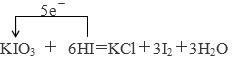 5:1
5:1
(2) 3 Fe + 8 HNO3(稀)= 3 Fe(NO3)2+ 2 NO↑+ 4 H2O 2:3

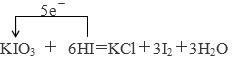 5:1
5:1(2) 3 Fe + 8 HNO3(稀)= 3 Fe(NO3)2+ 2 NO↑+ 4 H2O 2:3

试题分析:(1)根据方程式KIO3+6HI=KI+3I2+3H2O可知,KIO3中碘元素的化合价从+5价降低到0价,得到5个电子,因此KIO3是氧化剂。HI中碘元素的化合价从-1价升高到0价,失去1个电子,则HI是还原剂,所以根据电子得失守恒可知,还原剂与氧化剂的物质的量之比=5:1,则氧化产物与还原产物物质的量之比=5:1。
(2)根据方程式Fe +HNO3(稀)→Fe(NO3)2+NO↑+ H2O可知,反应中铁元素的化合价从0价升高到+2价失去2个电子。硝酸中氮元素的化合价从+5价降低到+2价得到3个电子,所以根据电子得失守恒可知,还原剂铁与氧化剂硝酸的物质的量之比=3:2,因此根据原子守恒可知,配平后的方程式为3Fe + 8HNO3(稀)=3Fe(NO3)2+2NO↑+ 4H2O。

练习册系列答案
相关题目
 Fe3O4+6SO2,有3mol FeS2参加反应,转移 mol电子。
Fe3O4+6SO2,有3mol FeS2参加反应,转移 mol电子。