题目内容
4.选择下列实验方法分离物质,将分离方法的字母填在横线上A.萃取分液法 B.加热分解法 C.重结晶法 D.分液法 E.蒸馏法 F.过滤法
(1)F分离饱和食盐水和沙子的混合物
(2)C从硝酸钾和氯化钠的混合溶液中获得硝酸钾
(3)E分离四氯化碳(沸点为76.75℃)和甲苯(沸点为110.6℃)的混合物
(4)D分离水和植物油的混合物.
分析 (1)沙子不溶于水;
(2)硝酸钾和氯化钠的溶解度受温度影响不同;
(3)四氯化碳和甲苯互溶,但沸点不同;
(4)水和植物油的混合物,分层.
解答 解:(1)沙子不溶于水,则选择过滤法分离,故答案为:F;
(2)硝酸钾和氯化钠的溶解度受温度影响不同,则选择结晶法分离,故答案为:C;
(3)四氯化碳和甲苯互溶,但沸点不同,则选择蒸馏法分离,故答案为:E;
(4)水和植物油的混合物,分层,则选择分液法你疯了,故答案为:D.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、性质差异、混合物分离方法为解答的关键,注侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案
相关题目
14.在25℃、1.01×105Pa下,将22g CO2通入到750mL 1.0mol•L-1的NaOH溶液中充分反应,放出x kJ热量.在该条件下1molCO2通入到2L 1.0mol•L-1的NaOH溶液中充分反应,放出ykJ热量,则CO2与NaOH反应生成NaHCO3的热化学反应方程式为( )
| A. | CO2(g)+NaOH(aq)═NaHCO3(aq)△H=-(2y-x) kJ•mol-1 | |
| B. | CO2(g)+NaOH(aq)═NaHCO3(aq)△H=-(4x-y) kJ•mol-1 | |
| C. | CO2(g)+NaOH(aq)═NaHCO3(aq)△H=-(2x-y) kJ•mol-1 | |
| D. | CO2(g)+NaOH(aq)═NaHCO3(aq)△H=-(8x-2y) kJ•mol-1 |
19.NH3是重要的化工原料.
(1)用NH4Cl和Ca(OH)2制备NH3,反应发生、气体收集和尾气处理装置依次为ACG或ADG.

(2)某学生用如图装置对NH3与NaClO的反应进行实验探究:
资料:氨和次氯酸钠溶液反应能生成肼.肼常温下是无色液体,沸点:113℃,与水混溶,它的水溶液是一种二元弱碱.
①向水中持续通入NH3,未观察到白雾.推测现象中的白雾由N2H4小液滴形成,进行实验:用湿润的红色石蕊试纸检验白雾,试纸变蓝.该实验不能判断白雾中含有N2H4,理由是白雾中混有NH3,NH3也可以使湿润的红色石蕊试纸变蓝.
②进一步实验确认了A中生成了N2H4.写出A中反应的化学方程式(N2不参与反应)2NH3+NaClO═N2H4+NaCl+H2O;此反应中若有5.6L氨气(标准状况下)参加反应,则转移电子的数目为0.25NA.
(1)用NH4Cl和Ca(OH)2制备NH3,反应发生、气体收集和尾气处理装置依次为ACG或ADG.

(2)某学生用如图装置对NH3与NaClO的反应进行实验探究:
| 操作 | 现象 |
 | 液面上方出现白雾 |
①向水中持续通入NH3,未观察到白雾.推测现象中的白雾由N2H4小液滴形成,进行实验:用湿润的红色石蕊试纸检验白雾,试纸变蓝.该实验不能判断白雾中含有N2H4,理由是白雾中混有NH3,NH3也可以使湿润的红色石蕊试纸变蓝.
②进一步实验确认了A中生成了N2H4.写出A中反应的化学方程式(N2不参与反应)2NH3+NaClO═N2H4+NaCl+H2O;此反应中若有5.6L氨气(标准状况下)参加反应,则转移电子的数目为0.25NA.
9.下列离子方程式改写成化学方程式正确的是( )
| A. | Cu2++2OH-═Cu(OH)2↓ CuCO3+2NaOH═Cu(OH)2↓+Na2CO3 | |
| B. | CO${\;}_{3}^{2-}$+2H+═CO2↑十H2O BaCO3+2HCl═BaCl2+C02↑十H20 | |
| C. | Ca2++CO${\;}_{3}^{2-}$═CaCO3↓ Ca(NO3)2+Na2CO3═CaCO3↓+2NaNO3 | |
| D. | H++OH-═H20 CH3COOH+KOH=CH3COOK+H20 |
16.在密闭容器中有可逆反应:nA(g)+mB(g)?pC(g);处于平衡状态(已知n+m>p,正反应为吸热反应),则下列说法正确的是:( )
①升温,c(B):c(C)的比值变小
②降温时体系内混合气体平均分子量变小
③加入B,A的转化率减小
④加入催化剂,气体总的物质的量不变
⑤加压使容器体积减小,体系内混合气体平均分子量一定增大
⑥若A的反应速率为vA,则B的反应速率vB=$\frac{n}{m}$vA.
①升温,c(B):c(C)的比值变小
②降温时体系内混合气体平均分子量变小
③加入B,A的转化率减小
④加入催化剂,气体总的物质的量不变
⑤加压使容器体积减小,体系内混合气体平均分子量一定增大
⑥若A的反应速率为vA,则B的反应速率vB=$\frac{n}{m}$vA.
| A. | ①②④⑤ | B. | ①②③⑤ | C. | ①②③⑥ | D. | ③④⑤⑥ |
13.下列反应中,属于氧化还原反应的是( )
| A. | CaCO3+2HCl═CaCl2+H2O+CO2↑ | B. | CaO+H2O═Ca(OH)2 | ||
| C. | Zn+H2SO4═ZnSO4+H2↑ | D. | H2CO3═H2O+CO2↑ |
14.下列变化需要加入还原剂才能实现的是( )
| A. | NH3→NH4+ | B. | Fe2+→Fe | C. | H2S→SO2 | D. | Cl-→Cl2 |

 的含氧官能团的名称为醚键和羧基、羟基
的含氧官能团的名称为醚键和羧基、羟基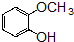 .
.