题目内容
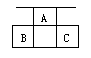
今有A、B、C、D、E五种短周期元素,它们的核电荷按 C、A、D、E的顺序增大。C、D都能分别与A按原子个数比1:1或2:1形成化合物。CB可与EA2反应生成C2A与气态物质EB4。
⑴写出五种元素名称A B ,C ,D , E 。
⑵画出E的原子结构简图 ,写出电子式D2A2 , EB4 。
⑶比较EA2与EB4的熔点高低 < 。
⑷写出D单质与CuSO4溶液反应的离子方程 。
⑴写出五种元素名称A B ,C ,D , E 。
⑵画出E的原子结构简图 ,写出电子式D2A2 , EB4 。
⑶比较EA2与EB4的熔点高低 < 。
⑷写出D单质与CuSO4溶液反应的离子方程 。
⑴氧,氟,氢,钠,硅 ⑵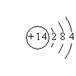 略
略
⑶ SiO2 >SiF4
⑷ 2Na+2H2O+Cu2+=Cu(OH)2↓+2Na++H2↑
 略
略 ⑶ SiO2 >SiF4
⑷ 2Na+2H2O+Cu2+=Cu(OH)2↓+2Na++H2↑
本题考查主族元素的化合价与原子序数的关系,以及有关元素周期表中各关系式的具体应用。此题的关键在于分析EB4中E元素只能是ⅣA族元素C或Si。因B 的原子序数不最小,则B不可能为H元素,E的价态应为+4,B应为ⅦA族元素,且只能为F,如果无Cl元素,则原子序数比E还大。而E只能为Si,即EB4为SiF4, 从CB的化合物的形式可知C为+1价,则由C2A可知A为-2价,只能为O。能与O按原子个数比1:1或2:1形成化合物的元素只能是H或Na。

练习册系列答案
相关题目