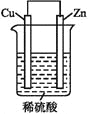
题目内容
【题目】有机物M可从酸牛奶中提取。已知纯净的M为无色黏稠液体, 易溶于水。为研究M的组成与结构,进行了如下实验:
实验步骤 | 解释或实验结论 |
(1)称取M4.5 g,升温使其汽化,测其密度是相同条件下H2的45倍。 | 试通过计算填空:(1)M的摩尔质量为: __ 。 |
(2)将此4.5 g M 在足量纯 O2中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重2.7g和6.6 g | (2)M的分子式为:____ 。 |
(3)通过M 的红外光谱图发现该分子中既有 羟基,还有羧基 | (3)写出M中含有的官能团羟基电子式:__ |
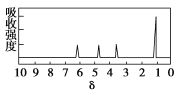
(4)M 的核磁共振氢谱如下图:
| (4)M 中含有___种氢原子。 |
(5)综上所述,M 的结构简式为_____ 。 | |
【答案】 90g/mol C3H6O3 ![]() 4
4 ![]()
【解析】试题分析:根据相同条件下密度比等于摩尔质量之比计算;产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重2.7g和6.6 g,可知燃烧生成水、二氧化碳分别是2.7g和6.6 g,根据元素守恒计算;羟基有1个没成对电子;根据M 的核磁共振氢谱图,可知M有4组峰,比值为1:1:1:3;
解析:(1)根据相同条件下密度比等于摩尔质量之比,其密度是相同条件下H2的45倍,所以摩尔质量是氢气的2倍,M的摩尔质量是90g/mol;(2) 燃烧生成水、二氧化碳分别是2.7g和6.6 g,氢元素的质量为0.3g、碳元素的质量为1.8g,所以4.5g M中元素的质量为2.4g,C、H、O的物质的量比为1:2:1,摩尔质量是90g/mol,所以分子式为C3H6O3;(2)羟基的电子式![]() ;(4)M中含有羟基、羧基,根据M 的核磁共振氢谱图,可知M有4组峰,即有4种等效氢,比值为1:1:1:3;(5)综上所述,M 的结构简式为
;(4)M中含有羟基、羧基,根据M 的核磁共振氢谱图,可知M有4组峰,即有4种等效氢,比值为1:1:1:3;(5)综上所述,M 的结构简式为![]() ;
;

 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案【题目】如表是A、B、C三种烃的有关信息;
A | B | C |
①能使溴的四氯化碳溶液褪色; ②比例模型为:
| ①平面型结构 ②棍模型为: | ①能使溴的四氯化碳溶液褪色; ②1mol能与2molH2在一定条件下反应生成A ③比例模型为: |
|
图2 |
根据表中信息回答下列问题:
(1)写出烃A与水反应的化学反应方程式_____________________;
(2)烃B分子碳碳键具有的特点是_______________________
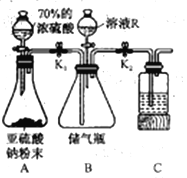
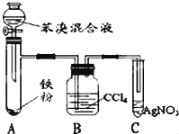
(3)如图1是烃B与液溴制取溴苯的装置,试回答:
(a)装置C中的现象___________________________________.
(b)装置B的作用__________________________________.
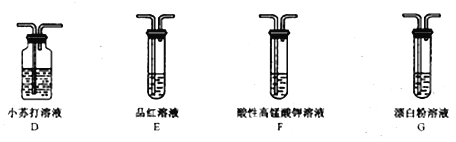
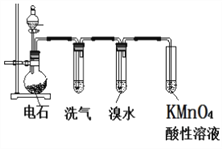
(4)如图2是制取烃C的装置,试回答:
(a)为了控制生成乙炔的速率,分液漏斗中盛放的液体是_______________。
(b)滴下液体后烧瓶中发生反应生成乙炔,写出此反应的化学方程式:_________。
(c)电石中含有硫化钙杂质,产生H2S,PH3等气体,为了不对乙炔性质造成干扰,应该除杂,一般选用___________洗气。