题目内容
【题目】实验室制备Cl2和新制的Cl2水,如图所示:
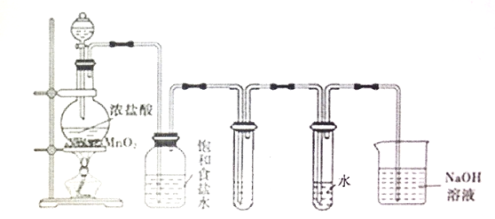
(1)装置中若无盛饱和食盐水的洗气瓶,将导致____________________。
(2)要证明Cl2与水反应是可逆反应,则证明Cl2水存在Cl2分子的现象是________,证明同时存在HCl和HClO的实验操作是_____________________。
(3)吸收Cl2尾气的化学反应方程式为________________________。
(4)用KClO3代替MnO2,不需加热就可以快速制得Cl2,该反应化学方程式为_____________________。
(5)有一种含氯氧化物,含氧量18.4%,与水反应,生成HClO,该氧化物的化学式是___________________,它属于___________。
A. 酸性氧化物 B. 碱性氧化物 C. 酸酐 D.氯化物
(6)新制氯水中加入少量Na2CO3溶液有气体产生,该反应的化学方程式为_____
【答案】Cl2中含有HCl气体 氯水呈黄绿色 取少量氯水滴加紫色石蕊试液,若出现先变红后褪色,则证明有HCl和HClO的存在(其它合理答案也给分) 2NaOH+Cl2=NaCl+NaClO+H2O KClO3+6HCl=KCl+3Cl2↑+3H2O Cl2O A、C 2Cl2+H2O+Na2CO3=CO2↑+2HClO+2NaCl
【解析】
(1)由于浓盐酸易挥发,生成的氯气中还有挥发出的氯化氢气体,可以用饱和食盐水除去氯化氢,因此若装置中若无盛饱和食盐水的洗气瓶,将导致Cl2中含有HCl气体。
(2)证明可逆反应,需验证在反应中反应物和生成物同时存在,氯气是黄绿色气体,则证明氯水中有Cl2存在的现象是氯水呈黄绿色;仅使用一种试剂证明氯水中HCl和HClO均存在,利用盐酸的酸性和次氯酸的漂白性,合适的试剂是石蕊试液,即取少量氯水滴加紫色石蕊试液,若出现先变红后褪色,则证明有HCl和HClO的存在。
(3)吸收Cl2尾气利用的是氢氧化钠溶液,反应的化学反应方程式为2NaOH+Cl2=NaCl+NaClO+H2O。
(4)用KClO3代替MnO2,不需加热就可以快速制得Cl2,根据原子守恒可知还有氯化钾和水生成,则该反应化学方程式为KClO3+6HCl=KCl+3Cl2↑+3H2O。
(5)有一种含氯氧化物,含氧量18.4%,则化合物中Cl、O的原子个数之比是![]() ,因此该氧化物的化学式是Cl2O。与水反应,生成HClO,次氯酸是含氧酸,且反应中元素化合价均不变,所以它属于酸性氧化物和酸酐,答案选AC。
,因此该氧化物的化学式是Cl2O。与水反应,生成HClO,次氯酸是含氧酸,且反应中元素化合价均不变,所以它属于酸性氧化物和酸酐,答案选AC。
(6)新制氯水中加入少量Na2CO3溶液有气体产生,气体是二氧化碳,由于盐酸的酸性强于碳酸,碳酸强于次氯酸,因此该反应的化学方程式为2Cl2+H2O+Na2CO3=CO2↑+2HClO+2NaCl。

 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案