题目内容
下列叙述正确的是( )
| A、离子晶体中可能含有非极性共价键 |
| B、原子晶体中的相邻原子间只存在非极性共价键 |
| C、分子晶体中一定含有共价键 |
| D、共价化合物中可能含有离子键 |
考点:离子化合物的结构特征与性质,共价键的形成及共价键的主要类型
专题:化学键与晶体结构
分析:A.离子晶体中可能含有非极性共价键,如Na2O2;
B.如为化合物,存在极性键;
C.单原子分子不存在共价键;
D.离子键只存在于离子化合物中.
B.如为化合物,存在极性键;
C.单原子分子不存在共价键;
D.离子键只存在于离子化合物中.
解答:
解:A.离子晶体中一定含有离子键,可能含有非极性共价键,如Na2O2,也可能含有极性共价键,如NaOH,故A正确;
B.SiO2晶体中存在极性键,故B错误;
C.单原子分子不存在共价键,如稀有气体,故C错误;
D.共价化合物只含有共价键,离子键只存在于离子化合物中,故D错误.
故选A.
B.SiO2晶体中存在极性键,故B错误;
C.单原子分子不存在共价键,如稀有气体,故C错误;
D.共价化合物只含有共价键,离子键只存在于离子化合物中,故D错误.
故选A.
点评:本题考查共价键和离子键以及晶体类型的判断,为高考常见题型和高频考点,侧重于学生的分析能力和基础知识的综合理解和运用的考查,难度不大,注意相关基础知识的积累.

练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目
下列离子方程式正确的是( )
| A、Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+═Fe3++3H2O |
| B、向NaHCO3溶液中加入少量Ca(OH)2溶液:2HCO+Ca2++2OH-═CaCO3↓+CO32-+2H2O |
C、向苯酚溶液中滴加Na2CO3溶液: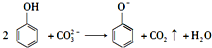 |
| D、向氯化亚铁溶液中滴加稀硝酸:Fe2++2H++NO═Fe3++NO2↑+H2O |
下列有关实验装置进行的相应实验,能达到实验目的是( )
A、 用如图所示装置进行稀硝酸与铜的反应制取并收集NO |
B、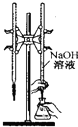 用如图所示装置进行用已知浓度的氢氧化钠溶液测定盐酸浓度的实验 |
C、 用如图所示装置制取少量Cl2 |
D、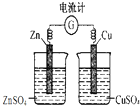 用如图所示装置检验电流的方向 |
在一定条件下,下列转化不能通过一步反应实现的是( )
| A、HCl→NaCl |
| B、CO→CaCO3 |
| C、Fe→FeSO4 |
| D、Ca(OH)2→NaOH |
下列叙述正确的是 ( )
| A、0.1mol/L CH3COONa溶液中:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| B、Na2CO3溶液加水稀释后,恢复至原温度,pH和Kw均减小 |
| C、pH=5的CH3COOH溶液和PH=5的NH4Cl溶液中,c(H+)不相等 |
| D、在Na2S溶液中加入AgCl固体,溶液中c(S2-)下降 |
有机物H 中不含有的官能团是( )
中不含有的官能团是( )
 中不含有的官能团是( )
中不含有的官能团是( )| A、醇羟基 | B、羧基 | C、醛基 | D、酯基 |
对于反应A2(g)+3B2(g)?2C(g);△H<0,则下列说法错误的是( )
| A、气体C的分子式为AB3 |
| B、使用催化剂能使平衡向生成C的方向移动,并放出更多的热量 |
C、A2,B2反应生成C,C的产率与温度.压强(P)关系的示意图如图: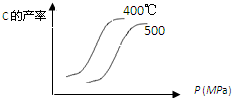 |
| D、恒温恒容时,若密闭容器内压强不变,表示反应已建立平衡 |
市场上销售的食品包装有多种方式,其中一种为真空包装,如香肠、盐水鸭、月饼等食品,抽出包装袋内空气并放入一小包铁粉.那么铁粉的主要表现的性质是( )
| A、氧化性 | B、还原性 |
| C、漂白性 | D、酸性 |