题目内容
常温下有A、B、C、D四种无色溶液,它们分别是CH3COONa溶液、NH4Cl溶液、盐酸和Na2SO4溶液中的一种。已知A、B溶液中水的电离程度相同,A、C溶液的pH相同。下列说法中不正确的是:( )
A.D溶液的pH=7
B.四种溶液相比,C溶液中水的电离程度最大
C.A与C等体积混合后,溶液中有c(Cl-)>c(NH4+) >c(H+) >c(OH-)
D.B与D等体积混合后,溶液中有c(OH-)=c(CH3COOH)+c(H+)
B
解析试题分析:已知A、B溶液中水的电离程度相同,可以判断A、C应该是二种能水解的盐;A、C溶液的pH相同,表明A、C应该是盐酸跟氯化铵溶液,所以A为NH4Cl溶液,B为CH3COONa溶液,C为盐酸,D为Na2SO4溶液,A、正确;B、C溶液为盐酸,对水的电离起到了抑制作用,水的电离子程度最小,错误;C、A与C等体积混合后,氯离子一定大于铵根离子,依据电荷守恒,c(Cl-)+c(OH-)=c(NH4+) +c(H+)可知,氢氧根离子一定小于氢离子,正确;D、B与D等体积混合后,依据质子守恒,溶液中有c(OH-)=c(CH3COOH)+c(H+),正确。
考点:考查溶液的有关知识。

pH=1的两种一元酸HX与HY溶液,分别取50 mL加入足量的镁粉,充分反应后,收集到H2体积分别为V(HX)和V(HY)。若V(HX)>V(HY),则下列说法正确的是
| A.HX可能是强酸 |
| B.HX的酸性比HY的酸性弱 |
| C.两酸的浓度大小[HX]<[HY] |
| D.pH=1的两种一元酸均稀释100倍,稀释后两溶液的pH均为3 |
室温时,0.1 mol·L-1的HA 溶液的pH=3,向该溶液中逐滴加入NaOH,在滴加过程中,有关叙述正确的是
| A.原HA溶液中,c(H+)=c(OH-)+c(A-) |
| B.当滴入少量的NaOH,促进了HA的电离,溶液的pH降低 |
| C.当恰好完全中和时,溶液中c(Na+)>c(A-)>c(OH-)>c(H+) |
| D.当NaOH溶液过量时,可能出现:c(A-)>c(Na+)>c(OH-)>c(H+) |
下列有关电解质溶液中微粒浓度关系不正确的是
A.0.lmol/LpH=4的NaHA溶液中: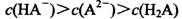 |
B.1mol/L的NaHCO3溶液中: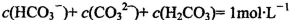 |
C.常温下,pH=7的NH4Cl与氨水的混合溶液中: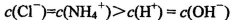 |
D.等体积、等物质的量浓度的NaX和弱酸HX的混合溶液中: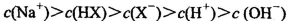 |
含有等物质的量NaOH的溶液分别用pH为2和3的CH3COOH溶液中和,设消耗CH3COOH溶液的体积依次为Va、Vb,则两者的关系正确的是( )
| A.Va>10 Vb | B.Va ="10" Vb |
| C.Vb >10 Va | D.Vb <10 Va |
常温下,0.1 mol·L-1的NaHB溶液中c(H+)>c(OH-),下列关系中一定正确的是( )
| A.c(Na+)+ c(H+)= c(HB-)+ 2c(B2-) | B.c(H+)·c(OH-)= 10-14 |
| C.c(Na+)= c(B2-)+ c(HB-) | D.溶液的pH=1 |
0.1 mol / L Na2CO3和0.1 mol / L NaHCO3溶液的pH值比较( )
| A.大于 | B.等于 | C.小于 | D.不能肯定 |
下列应用与盐类的水解无关的是 ( )
| A.NaCl可用作防腐剂和调味剂 | B.明矾净水 |
| C.泡沫灭火器的灭火原理 | D.FeCl3饱和溶液滴入沸水中制备Fe(OH)3胶体 |