题目内容
粗CuO是将工业废铜、废铜合金等高温焙烧而成的,杂质主要是铁的氧化物及泥沙。以粗CuO为原料制备胆矾的主要流程如下: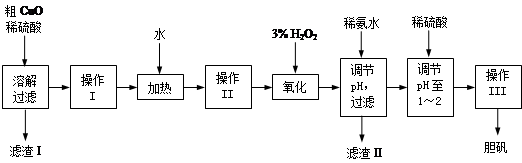
经操作I得到粗胆矾,操作III得到精制胆矾。两步操作相同,具体包括蒸发浓缩、冷却结晶、过滤、洗涤、干燥等步骤。
已知: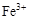 、
、 、
、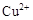 转化为相应氢氧化物时,开始沉淀和沉淀完全时的pH如下表:
转化为相应氢氧化物时,开始沉淀和沉淀完全时的pH如下表:
| | 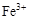 |  | 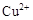 |
| 开始沉淀时的pH | 2.7 | 7.6 | 5.2 |
| 完全沉淀时的pH | 3.7 | 9.6 | 6.4 |
(1)溶解、过滤需要用到玻璃棒,它的作用是 。
(2)写出加入3% H2O2后发生反应的离子方程式 。(原溶液显酸性)。
(3)加稀氨水调节pH应调至范围 。下列物质可用来替代稀氨水的是 。(填字母)
A.NaOH B.Cu(OH)2 C.CuO D.NaHCO3
(4)操作III析出胆矾晶体后,溶液中还可能存在的溶质为CuSO4、H2SO4、________________。
(5)某学生用操作III所得胆矾进行“硫酸铜晶体结晶水含量”的测定,数据记录如下表所示:
| | 第一次实验 | 第二次实验 |
| 坩埚质量(g) | 14.520 | 14.670 |
坩埚质量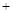 晶体质量(g) 晶体质量(g) | 17.020 | 18.350 |
| 第一次加热、冷却、称量(g) | 16.070 | 16.989 |
| 第二次加热、冷却、称量(g) | 16.070 | 16.988 |
(填字母)。
A.加热前称量时坩埚未完全干燥 B.该胆矾中含有受热不分解的杂质
C.加热后坩埚放在干燥器中冷却 D.玻璃棒上沾有的固体未刮入坩埚
(1)搅拌、引流 (1分)
(2)2Fe2+ +H2O2 +2H+ →2Fe3+ +2H2O (2分)
(3)3.7~5.2 (1分) ; BC(2分)
(4)(NH4)2SO4或NH4HSO4 (1分,写到一个即给分)
(5)已达恒重 (1分);+4.2% (2分);AD (2分)
解析试题分析:(1)溶解、过滤需要用到玻璃棒,它的作用是搅拌、引流。
(2)由于双氧水不稳定,加热易分解生成氧气和水。由于在加入双氧水之前溶液的温度较高,所以加入3% H2O2之前必须进行冷却操作。由于亚铁离子沉淀的pH较大,所以必须将其氧化成铁离子沉淀,因此加入双氧水的目的是氧化亚铁离子,反应的离子方程式为2Fe2+ + H2O2 + 2H+= 2Fe3+ +2H2O。
(3)要得到胆矾,就必须除去溶液中的铁离子,则根据沉淀时的pH值可知,调节溶液pH的目的是使Fe3+完全转变成Fe(OH)3沉淀;铁离子完全沉淀时的pH=3.7,而铜离子开始沉淀时的pH=5.2,所以溶液的pH应调节到3.7~5.2之间。由于在调节pH的同时,不能引入杂质,因此应该选择氧化铜,Cu(OH)2 来调节溶液的pH。
(4)操作III析出胆矾晶体后,溶液中还可能存在的溶质为CuSO4、H2SO4、(NH4)2SO4或NH4HSO4。
(5)根据表中的数据两次实验都已达恒重故没必要再进行第三称量。坩埚质量(g)(14.52+14.67)/2=" 14.595" 实验1:晶体质量:17.02-14.595=2.425水的质量:17.02-16.07=0.95,水的质量分数:0.95/2.425=0.3917,实验2:晶体质量:18.35-14.595=3.755水的质量:18.35-16.99=1.36,水的质量分数:1.36/3.755=0.3622,两次平均水的质量分数:0.3769,五水硫酸铜中水的理论质量数:0.36,相对误差(0.3769-0.360/0.36=0.042。产生实验误差是偏大,即水的质量较多或剩余固体的质量较少,其原因可能是A.加热前称量时坩埚未完全干燥有了多余的水,正确。B.该胆矾中含有受热不分解的杂质会使结果偏低。C.加热后坩埚放在干燥器中冷却,不会带来误差。D.玻璃棒上沾有的固体未刮入坩埚,有一部分固体没有得到称量,相当于剩余的固体质量减小,正确。
考点:考查胆矾制备实验设计与探究以及实验相对误差的分析处理等

某种粗盐中含有泥沙、Ca2+、Mg2+、Fe3+、SO等杂质。某同学在实验室中设计了用这种粗盐制备精盐的方案如下(用于沉淀的试剂稍过量):
请回答以下问题:
(1)为操作Ⅳ选择所需仪器(用标号字母填写):________。
| A.烧杯 | B.试管 | C.玻璃棒 | D.分液漏斗 E.漏斗 F.酒精灯 |
(2)操作Ⅲ中常用Na2CO3溶液、NaOH溶液、BaCl2溶液作为除杂试剂,则加入除杂试剂的顺序为:NaOH溶液→________→________。
(3)操作Ⅲ中,判断加入BaCl2已过量的方法是_________________________。
(4)操作Ⅴ应选择的酸是________,若将操作Ⅴ与操作Ⅳ的先后顺序对调,将会对实验结果产生的影响是__________________________________________。
(5)操作Ⅵ是________(选择合理操作的名称,用标号字母按操作先后顺序填写)。
a.过滤、洗涤 b.蒸发、浓缩 c.萃取、分液 d.冷却、结晶
草酸(H2C2O4)是一种弱酸,在工业中有重要作用。某同学查资料得知“菠菜中富含可溶性草酸盐和碳酸盐”,他将菠菜研磨成汁,热水浸泡,经过滤得到溶液,加入足量的CaCl2溶液,产生白色沉淀,过滤、洗涤沉淀备用,然后对生成的沉淀进行探究。
(1)草酸盐溶液呈弱碱性的原因是_____________________________________。
(2)该同学对生成的沉淀进行定性探究。
①提出合理假设。
假设1:只存在CaCO3;
假设2:既存在CaCO3,也存在CaC2O4;
假设3:___________________________________________________________。
②基于假设2,设计实验方案,进行实验。请在下表中写出实验步骤以及预期现象和结论。限选实验试剂:
1 mol·L-1 H2SO4、0.1 mol·L-1盐酸、0.01 mol·L-1 KMnO4溶液、澄清石灰水。
| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量沉淀于试管中,加入_________________________________ ________________________________ | _______________________________ _______________________________ 说明沉淀中有CaCO3 |
| 步骤2:_________________________ ________________________________ | ________________________________ |
(3)基于假设3,另一位同学对生成的沉淀进行定量探究。用稀盐酸溶解生成的沉淀,并加水配制成100 mL溶液。每次准确移取25.00 mL该溶液,用0.010 mol·L-1 KMnO4标准溶液滴定,平均消耗标准溶液V mL。若菠菜样品的质量为m g,则菠菜中草酸及草酸盐(以C2O42—计)的质量分数为________。
实验室制取乙烯的反应原理为:CH3CH2OH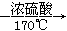 CH2=CH2↑+H2O,反应时,常因温度过高而使乙醇和浓H2SO4反应生成少量的SO2,有人设计下列实验确认上述混合气体中有乙烯和二氧化硫。
CH2=CH2↑+H2O,反应时,常因温度过高而使乙醇和浓H2SO4反应生成少量的SO2,有人设计下列实验确认上述混合气体中有乙烯和二氧化硫。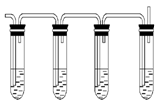
试回答下列问题:
(1)图中①②③④装置盛放的试剂分别是(填选项字母):①_________,④_________。
| A.品红溶液 | B.NaOH溶液 | C.浓硫酸 | D.酸性高锰酸钾溶液 |
(3)确证乙烯存在的现象是_______________________________________________________________。