题目内容
20.某种有机物的分子模型如图,图中的“棍”代表单键或双键,该模型代表的有机物可能是( )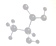
| A. | 饱和一元醇 | B. | 羟基酸 | C. | 羧酸 | D. | 饱和一元醛 |
分析 由球棍模型可知,此有机物中存在三种元素,且正键特点为四个和两个以及1个,据此可以判断该有机物的结构.
解答 解: ,由此球棍模型可知,有机物中存在三种元素,且正键特点为四个和两个以及1个,故此有机物可能为羟基酸,故选B.
,由此球棍模型可知,有机物中存在三种元素,且正键特点为四个和两个以及1个,故此有机物可能为羟基酸,故选B.
点评 本题主要考查的是球棍模型,球棒模型是一种空间填充模型,用来表现化学分子的三维空间分布.在此作图方式中,线代表共价键,可连结以球型表示的原子中心,难度不大.

练习册系列答案
相关题目
11.哈伯因发明了由氮气和氢气合成氨气的方法而获得1918年诺贝尔化学奖,现向一密闭容器中充入N2和H2,在一定条件下使该反应发生,有关说法正确的是( )
N2+3H2$?_{高温、高压}^{催化剂}$2NH3.
N2+3H2$?_{高温、高压}^{催化剂}$2NH3.
| A. | 达到化学平衡时,N2完全转化为NH3 | |
| B. | 达到化学平衡时,正反应和逆反应的速率都为零 | |
| C. | N2、H2和NH3的物质的量浓度不再变化时,反应达到平衡 | |
| D. | 单位时间内每增加1molN2,同时增加3molH2时,反应达到化学平衡 |
8.反应A(g)+B(g)═C(g),在5s内A的浓度由6.0mol/L变成2.0mol/L,此5s内用C表示的反应速率为( )
| A. | 0.8mol/(L.s) | B. | 2.0mol/(L.s) | C. | 4.0mol/(L.s) | D. | 6.0mol/(L.s) |
5.下列离子方程式正确的是( )
| A. | 钠与水反应:Na+H2O═Na++OH-+H2↑ | |
| B. | 小苏打与氢氧化钠溶液混合:HCO3-+OH-═CO2↑+H2O | |
| C. | 苯酚钠溶液中通入少量CO2:CO2+H2O+2C6H5O-→2C6H5OH+2CO32- | |
| D. | 氧化亚铁溶液中加入稀硝酸:3FeO+10H++NO3-═3Fe3++NO↑+5H2O |
12.设NA为阿伏伽德罗常数,下列叙述正确的是( )
| A. | 1mol烃基中电子数为10NA | |
| B. | 标准状况下,11.2L乙醇中含有的分子数为0.5NA | |
| C. | 标准状况下,0.56L丙烷中含有共价键的数目为0.2NA | |
| D. | 0.1mol乙烯和乙醇的混合物完全燃烧所消耗的氧原子数一定为0.6NA |
9.某种芳香族化合物的分子式为C8H10O,其中与FeCl3溶液混合后显色与不显色的结构分别有( )
| A. | 6种和6种 | B. | 6种和3种 | C. | 9种和10种 | D. | 9种和5种 |
10.下列仪器的使用方法或实验操作正确的是( )
| A. | 烧杯、量筒、容量瓶用于溶液配制时,均可直接溶解溶质 | |
| B. | 受热的试管、烧杯、坩埚、蒸发皿均可放在实验台上冷却 | |
| C. | 容量瓶、滴定管、长颈漏斗使用前均要检漏 | |
| D. | 用托盘天平称量纯碱、胆矾、食盐时,在两托盘上垫等大的白纸称量 |