题目内容
10.高锰酸钾是锰的重要化合物和常用氧化剂,在实验室和医疗上有非常广泛的应用.图1是工业上用软锰矿(主要含MnO2)制备高锰酸钾晶体的一种工艺流程: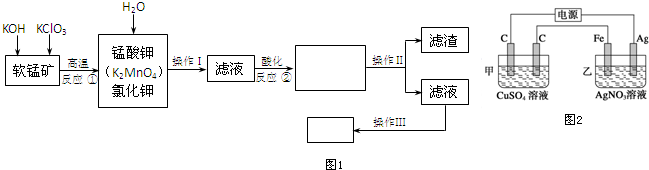
(1)操作Ⅱ的名称是过滤,实验室进行该操作须用到的玻璃仪器有烧杯、漏斗、玻璃棒;
(2)反应②的产物中,氧化产物与还原产物的物质的量之比是2:1;
(3)反应②中“酸化”时不能选择下列酸中的a(填字母序号)
a.稀盐酸 b.稀硫酸 c.稀醋酸
(4)用如图2所示的装置进行电解,在通电一段时间后,铁电极的质量增加.
①写出乙中两极发生的电极反应式.
阴极:Ag++e-=Ag;
阳极:Ag-e-=Ag+.
②写出甲中发生反应的化学方程式:2CuSO4+2H2O$\frac{\underline{\;电解\;}}{\;}$2Cu+O2↑+2H2SO4.
③C(左)、C(右)、Fe、Ag 4个电极上析出或溶解物质的物质的量之比是2:1:4:4.
分析 根据流程图知,软锰矿(主要含MnO2)和KOH和氯酸钾高温反应生成K2MnO4,3MnO2+6KOH+KClO3 $\frac{\underline{\;高温\;}}{\;}$3K2MnO4+3H2O+KCl,加入水通过过滤,分离出杂质,滤液中含K2MnO4、KCl,滤液酸化,K2MnO4与酸发生氧化还原反应生成KMnO4和MnO2,过滤得到滤液蒸发浓缩冷却结晶过滤洗涤的高锰酸钾;
(1)软锰矿中含有不溶于水的物质,由流程图可知,通过操作Ⅰ得到滤液,因此操作Ⅰ为过滤;(2)K2MnO4与酸发生氧化还原反应生成KMnO4和MnO2,由化合价升降相等确定氧化产物与还原产物的物质的量之比;
(3)酸性高锰酸钾溶液能氧化盐酸,因此不能选用盐酸酸化;
(4)①装置是电解池,通电一段时间后发现乙烧杯中铁电极的质量增加,铁做电解池阴极,银做阳极;
②甲烧杯中和铁连接的为阳极,左边的碳棒是阴极,电解硫酸铜溶液生成铜、氧气和硫酸;
③阳极电极反应和电子守恒计算电极产物或电解溶解的物质的量.
解答 解:根据流程图知,软锰矿(主要含MnO2)和KOH和氯酸钾高温反应生成K2MnO4,3MnO2+6KOH+KClO3 $\frac{\underline{\;高温\;}}{\;}$3K2MnO4+3H2O+KCl,加入水通过过滤,分离出杂质,滤液中含K2MnO4、KCl,滤液酸化,K2MnO4与酸发生氧化还原反应生成KMnO4和MnO2,过滤得到滤液蒸发浓缩冷却结晶过滤洗涤的高锰酸钾;
(1)由流程图可知,通过操作Ⅱ得到滤液、滤渣,因此操作Ⅱ为过滤,过滤用到的玻璃仪器有:玻璃棒、漏斗、烧杯,
故答案为:过滤;烧杯、漏斗、玻璃棒;
(2)K2MnO4与酸发生氧化还原反应生成KMnO4和MnO2,Mn元素的化合价由+6变为+7和+4价,因此KMnO4为氧化产物,MnO2为还原产物,根据化合价升降相等可知,氧化产物与还原产物的物质的量之比为(6-4):(7-6)=2:1,
故答案为:2:1;
(3)酸性高锰酸钾溶液能氧化盐酸生成氯气,因此不能选用盐酸酸化,故答案为:a;
(4)①通电一段时间后发现乙烧杯中铁电极的质量增加,铁做电解池阴极,银做阳极,电解质溶液是硝酸银溶液,所以原理是电镀原理,阴极电极反应为:Ag++e-=Ag;阳极电极反应为:Ag-e-=Ag+,
故答案为:Ag++e-=Ag;Ag-e-=Ag+;
②甲烧杯中和铁连接的为阳极,左边的碳棒是阴极,电解硫酸铜溶液生成铜、氧气和硫酸,电池反应为:2CuSO4+2H2O$\frac{\underline{\;电解\;}}{\;}$2Cu+O2↑+2H2SO4,
故答案为:2CuSO4+2H2O$\frac{\underline{\;电解\;}}{\;}$2Cu+O2↑+2H2SO4;
③甲中阴极电极反应为2Cu2++4e-=2Cu,阳极电极反应为4OH--4e-=2H2O+O2↑;乙池中电极反应,阳极电极反应为4Ag-4e-=4Ag+;阴极电极反应为4Ag++4e-=4Ag;依据电子守恒计算得到,由左到右碳-碳-铁-银四个是极上析出或溶解物质的物质的量之比是2:1:4:4,
故答案为:2:1:4:4.
点评 本题考查了常见氧化剂与还原剂、氧化还原反应计算和对工艺流程的理解、阅读题目获取信息的能力、电解池原理的应用等,关键是弄清过程和步骤的目的,理解信息和物质性质,(4)主要是电极判断,电极反应,电极产物的分析判断,电子守恒的计算应用,题目难度中等.

 阅读快车系列答案
阅读快车系列答案| A. | 14C的原子结构示意图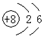 | B. | H2O2的电子式: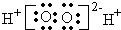 | ||
| C. | CO2的比例模型: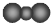 | D. | HClO的结构式:H-O-Cl |
| 温度/℃ | 250 | 310 | 350 |
| K/(mol•L-1)-2 | 2.041 | 0.250 | 0.012 |
(2)某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应达到平衡后,测得c(CO)=0.5mol•L-1,则此时的温度为310℃.
(3)在容积固定的密闭容器中发生上述反应,各物质的浓度如下表:
| 浓度mol•L-1 时间/min | C(CO) | C(H2) | C(CH3OH) |
| 0 | 0.8 | 1.6 | 0 |
| 2 | 0.6 | x | 0.2 |
| 4 | 0.3 | 0.6 | 0.5 |
| 6 | 0.3 | 0.6 | 0.5 |
②反应达到平衡时CO的转化率为62.5%.
③反应在第2min时改变了反应条件,改变的条件可能是a(填序号).
a.使用催化剂 b.降低温度 c.增加H2的浓度
(4)常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H=-1275.6kJ•mol-1
②2CO(g)+O2(g)=2CO2(g)△H=-566.0kJ•mol-1
③H2O(g)=H2O(l)△H=-44.0kJ•mol-1
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:CH3OH(l)+O2(g)=CO(g)+2H2O(l)△H=-442.8kJ•mol-1
(5)一种甲醇燃料电池中发生的化学反应为:在酸性溶液中甲醇与氧化作用生成水和二氧化碳.该电池的负极反应式为:CH3OH+H2O=CO2+6H++6e-.若以上述燃料电池为电源来电解饱和食盐水,当消耗32g甲醇时,电解产生的H2体积(标况)为67.2 L.
| A. | 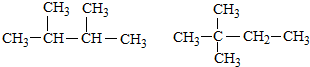 | |
| B. | 液氯、氯气 | |
| C. | O2、O3 | |
| D. | ${\;}_{17}^{35}Cl$、${\;}_{17}^{37}Cl$ |
| A. | 在含有Fe3+大量的溶液中:NH4+、Na+、Cl-、SCN- | |
| B. | 某无色透明溶液:NH4+、K+、SO32-、Cr2O72- | |
| C. | 在c(H+)=0.1mol/L的溶液中:K+、Mg2+、Cl-、NO3- | |
| D. | 在能与Al反应产生H2的溶液中:NH4+、NO3-、SO42-、HCO3- |
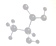
| A. | 饱和一元醇 | B. | 羟基酸 | C. | 羧酸 | D. | 饱和一元醛 |