题目内容
草酸(乙二酸)可作还原剂和沉淀剂,用于金属除锈、织物漂白和稀土生产。一种制备草酸(含2个结晶水)的工艺流程如图:回答下列问题:
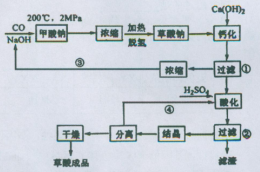
(1)CO和NaOH在一定条件下合成甲酸钠,甲酸钠加热脱氢的化学反应方程式分别为:____、____ 。
(2)该制备工艺中有两次过滤操作,过滤操作①的滤液是 ,滤渣是____ ;过滤操作②的滤液是 和 ,滤渣是____ 。
(3)工艺过程中③和④的目的是____ 。
(4)有人建议甲酸钠脱氢后直接用硫酸酸化制备草酸。该方案的缺点是产品不纯,其中含有的杂质主要是___ 。
(5)结晶水合草酸成品的纯度用高锰酸钾法测定。
称量草酸成品0.250 g溶于水,用0.0500 mol·L-1的酸性KMn04溶液滴定,至浅粉红色不消褪,消耗KMn04溶液15.00 mL,反应的离子方程式为____ ;
列式计算该成品的纯度 。

(1)CO和NaOH在一定条件下合成甲酸钠,甲酸钠加热脱氢的化学反应方程式分别为:____、____ 。
(2)该制备工艺中有两次过滤操作,过滤操作①的滤液是 ,滤渣是____ ;过滤操作②的滤液是 和 ,滤渣是____ 。
(3)工艺过程中③和④的目的是____ 。
(4)有人建议甲酸钠脱氢后直接用硫酸酸化制备草酸。该方案的缺点是产品不纯,其中含有的杂质主要是___ 。
(5)结晶水合草酸成品的纯度用高锰酸钾法测定。
称量草酸成品0.250 g溶于水,用0.0500 mol·L-1的酸性KMn04溶液滴定,至浅粉红色不消褪,消耗KMn04溶液15.00 mL,反应的离子方程式为____ ;
列式计算该成品的纯度 。

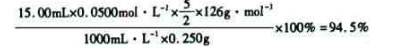
试题分析:⑴CO和NaOH在一定条件下合成甲酸钠的反应可用观察法将其配平;甲酸钠加热脱氢(产生H2),通过观察法并结合原子守恒得另一生成物为Na2C2O4。
⑵根据“钙化”反应:Na2C2O4+Ca(OH)2=CaC2O4↓+2NaOH,由此可确定过滤操作①的滤液是NaOH,滤渣是CaC2O4;根据“酸化”反应:CaC2O4+H2SO4=CaSO4+ H2C2O4,由此可确定过滤操作②的滤液是H2C2O4,滤渣是CaSO4;
⑶该工艺过程中③和④(“回头”)分别循环利用氢氧化钠和硫酸,减小污染,也可降低成本。
⑷若在甲酸钠脱氢后生成的Na2C2O4中直接用硫酸酸化制备草酸,会产生Na2SO4杂质。
⑸根据得失电子守恒有5C2O42-+2MnO4-――2Mn2++10CO2↑,再根据电荷守恒有5C2O42-+2MnO4-+16H+――2Mn2++10CO2↑,最后根据原子守恒得5C2O42-+2MnO4-+16H+=2Mn2++10CO2↑+8H2O;最后根据该反应方程式建立关系式“5(H2C2O4·2H2O)~2KMnO4”,得该成品的纯度为:
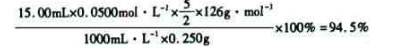 。
。
练习册系列答案
相关题目
 、SO32—、SO42—、Fe2+、Fe3+、K+,按如下流程进行实验:
、SO32—、SO42—、Fe2+、Fe3+、K+,按如下流程进行实验: