题目内容
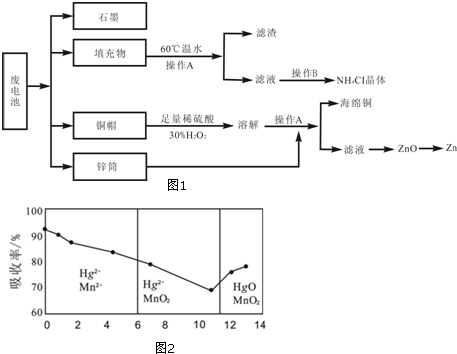
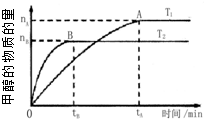
5.可逆反应①X(g)+2Y(g)?2Z(g)、②2M(g)?N(g)+P(g)分别在密闭容器的两个反应室中进行,反应室之间有无摩擦、可滑动的密封隔板.反应开始和达到平衡状态时有关物理量的变化如图所示:
(1)反应①的正反应△H<0(填“>”、“=”或“<”);
(2)达平衡(Ⅰ)时体系的压强与反应开始时体系的压强之比为20:23;(用分数表示)
(3)达平衡(Ⅰ)时,X的转化率为$\frac{15}{23}$;(用分数表示)
(4)在平衡(Ⅰ)和平衡(Ⅱ)中,M的体积分数(Ⅰ)无法确定(Ⅱ) (填“>”、“=”、“<”或
“无法确定”).
分析 (1)根据右室的混合物总物质的量不变,平衡(I)、平衡(Ⅱ)左右两室的温度、压强相同,体积之比等于物质的量之比,结合图示容器容积变化判断降温后反应①平衡移动的方向;
(2)根据右室的混合物总物质的量不变,在同温同压下体积比等于物质的量之比计算出反应后(I)中混合气体的物质的量,再计算出达平衡(I)时体系的压强与反应开始时体系的压强之比;
(3)设参加反应的X的物质的量为amol,利用差量法计算a的值,再利用转化率定义计算A的转化率;
(4)根据右边反应2M(g)?N(g)+P(g)气体的总物质的量不变,温度变化,平衡移动判断在平衡(I)和平衡(II)中M的体积分数是否相等.
解答 解:(1)右室的混合物总物质的量不变,平衡(I)、平衡(Ⅱ)左右两室的温度、压强相同,体积之比等于物质的量之比,由图可知,平衡(I)降低温度达新平衡平衡(Ⅱ),隔板由2.7处移至2.6处,左室的气体的物质的量减小,降低温度平衡向正反应移动,降低温度平衡向放热反应移动,故该反应正反应为放热反应,
故答案为:<;
(2)右室的混合物总物质的量不变为2mol,左右两室的压强、温度相等,同温同压下,体积之比等于物质的量之比,平衡(I)中左室混合气体总的物质的量为$\frac{2.7}{2.3}$×2mol=$\frac{54}{23}$mol,反应过程中温度不变,根据PV=nRT可知:P=$\frac{n}{V}$RT,所以达平衡(I)时体系的压强与反应开始时体系的压强之比为:$\frac{\frac{54}{23}}{2.7}$:$\frac{3}{3}$=20:23,
故答案为:20:23;
(3)根据(2)可知,平衡(I)中左室混合气体总的物质的量为$\frac{54}{23}$mol,设参加反应的X的物质的量为amol,则:
X(g)+2Y(g)?2Z(g) 物质的量减少△n
1 1
amol (3mol-$\frac{54}{23}$mol)=$\frac{15}{23}$mol
解得a=$\frac{15}{23}$mol,所以X的转化率为$\frac{\frac{15}{23}mol}{1mol}$=$\frac{15}{23}$,
故答案为:$\frac{15}{23}$;
(4)右室中气体的总物质的量始终不变,但是由于降低温度,反应2M(g)?N(g)+P(g)的平衡发生移动,导致M的含量变化,所以在平衡(I)和平衡(II)中M的体积分数不相等,
故答案为:无法确定.
点评 本题考查化学平衡移动与化学计算,题目难度中等,是对知识的综合运用,需要学生具备扎实的基础知识与运用知识分析问题、解决问题的能力,( II)中清楚左右两室的温度、压强相同,体积之比等于物质的量之比是解题关键.

 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案| A. | 金属钠暴露在空气中,表面变暗,生成淡黄色固体 | |
| B. | 用坩埚钳夹住打磨过的镁带,在酒精灯上点燃,发出耀眼的黄光 | |
| C. | 用坩埚钳夹住铝箔在酒精灯上加热至熔化,轻轻晃动,有液态的铝滴落 | |
| D. | 钠常常保存在石蜡油或煤油中 |
| A. | 向NaHSO3溶液中加入NaHSO4溶液:HSO${\;}_{3}^{-}$+H+═H2O+SO2↑ | |
| B. | 铁溶于稀硝酸,溶液变黄:3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O | |
| C. | Ba(OH)2与H2SO4两稀溶液混合:Ba2++2OH-+2H++SO${\;}_{4}^{2-}$═BaSO4↓+2H2O | |
| D. | AlCl3溶液中加入过量氨水:Al3++3NH3•H2O═Al(OH)3↓+3NH${\;}_{4}^{+}$ |
| 容器 编号 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |
| A(g) | B(g) | C(g) | ||
| Ⅰ | 387 | 0.20 | 0.080 | 0.080 |
| Ⅱ | 387 | 0.40 | ||
| Ⅲ | 207 | 0.20 | 0.090 | 0.090 |
| A. | 该反应的正反应为放热反应 | |
| B. | 达到平衡时,容器Ⅰ中的A体积分数与容器Ⅱ中的相同 | |
| C. | 容器Ⅰ中反应到达平衡所需时间比容器Ⅲ中的短 | |
| D. | 若起始时向容器Ⅰ中充入0.15 mol A、0.15 mol B 和0.10 mol C则反应将向逆反应方向进行 |
| A. | 催化剂 | B. | 温度 | C. | 浓度 | D. | 压强 |

 科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池.已知H2(g)、CO(g)和CH3OH(l )的燃烧热△H分别为-285.8kJ•mol-1、-283.0kJ•mol-1和-726.5kJ•mol-1.请回答下列问题:
科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池.已知H2(g)、CO(g)和CH3OH(l )的燃烧热△H分别为-285.8kJ•mol-1、-283.0kJ•mol-1和-726.5kJ•mol-1.请回答下列问题: