题目内容
铬是人体必需的微量元素,但铬过量会引起污染,危害人体健康。不同
价态的铬毒性不一样,六价铬的毒性最大。下列叙述错误的是( )
| A.K2Cr2O7可以氧化乙醇,可用来鉴别司机是否酒后驾驶 |
| B.污水中铬一般以Cr3+存在,与水中的溶解氧作用可被还原为六价铬 |
| C.人体内六价铬超标,服用维生素C缓解毒性,说明维生素C具有还原性 |
| D.1 mol Cr2O72—得到6 mol电子时,还原产物是Cr3+ |
B
解析

练习册系列答案
相关题目
在下列反应中,HCl作还原剂的是( )
| A.2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O |
| B.Zn+2HCl=ZnCl2+H2↑ |
| C.NaOH+HCl=NaCl+H2O |
| D.CuO+2HCl=CuCl2+H2O |
氢化亚铜(CuH)是一种不稳定物质,能在氯气中燃烧;也能与酸反应。用CuSO4溶液和“某物质”在40~50℃时反应可产生它。下列有关叙述中错误的是
| A.这“某物质”具有还原性 |
| B.CuH与盐酸反应,可能产生H2 |
| C.CuH与足量的稀硝酸反应:CuH + 3H+ + NO3—= Cu2++ NO↑+ 2H2O |
| D.CuH在氯气中燃烧:CuH + Cl2=" CuCl" + HCl |
工业上粗硅的生产原理为2C+SiO2 Si+2CO↑,下列说法正确的是
Si+2CO↑,下列说法正确的是
| A.SiO2是氧化剂 | B.SiO2发生氧化反应 |
| C.C表现出氧化性 | D.C被还原 |
用0.1 mol/L的Na2SO3溶液30 mL,恰好将2×10-3 mol XO4-还原,则元素X在还原产物
中的化合价是
| A.+4 | B.+3 | C.+2 | D.+1 |
铜的冶炼大致可分为:
(1)富集,将硫化物矿进行浮选
(2)焙烧,主要反应:2CuFeS2+4O2=Cu2S+3SO2+2FeO(炉渣)
(3)制粗铜,在1200 ℃发生的主要反应:2Cu2S+3O2=2Cu2O+2SO2;2Cu2O+Cu2S=6Cu+SO2↑
(4)电解精炼
下列说法正确的是
| A.上述焙烧过程的尾气均可直接排空 |
| B.由6 mol CuFeS2生成6 mol Cu,上述共消耗15 mol O2 |
| C.在反应2Cu2O+Cu2S=6Cu+SO2↑中,作氧化剂的只有Cu2O |
| D.电解精炼时,粗铜应与外电源负极相连 |
将a g铝粉加入过量NaOH溶液中充分反应后,铝粉完全溶解,并收集到标准状况下b L氢气,所得溶液中共有c个AlO2-,反应中转移电子d个。则阿伏加德罗常数(NA)可表示为( )
A.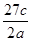 | B.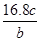 | C.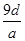 | D.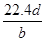 |
工业上以铬铁矿(主要成分为FeO·Cr2O3)、碳酸钠、氧气和硫酸为原料生产重铬酸钠
(Na2Cr2O7·2H2O),其主要反应:( )
①4FeO·Cr2O3+8Na2CO3+7O2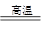 8Na2CrO4+2Fe2O3+8CO2 ②2Na2CrO4+H2SO4
8Na2CrO4+2Fe2O3+8CO2 ②2Na2CrO4+H2SO4 Na2SO4+Na2Cr2O7+H2O
Na2SO4+Na2Cr2O7+H2O
下列说法不正确的是( )
| A.反应①和②均为氧化还原反应 |
| B.Na2Cr2O7在碱性条件下可转化为Na2CrO4 |
| C.高温下,O2的氧化性大于Fe2O3和Na2CrO4的 |
| D.生成1 mol Na2Cr2O7时转移电子的物质的量大于7 mol |
美国宇航局“凤凰”号火星登陆器的显微、电子化学及传导分析仪对两份土壤样本的分析发现,火星北极区表层土壤可能含有高氯酸盐,可创造不利于任何潜在生命的恶劣环境。则下列说法错误的是 ( )
| A.含有高氯酸盐的土壤不利于生命存在与高氯酸盐具有较强的氧化性有关 |
| B.当元素处于最高价态时一定具有强氧化性 |
| C.可以考虑用加入亚铁盐等还原性物质的方法改善这种土壤 |
| D.一定条件下高氯酸盐能与浓盐酸反应生成氯气 |