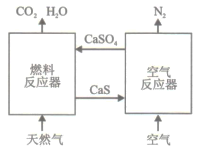
题目内容
【题目】有机物A 气体为直线型分子;B、C气体在标况下的密度均为1.25g/L;反应①②反应机理类似且原子利用率均为 100%;请回答下列问题:
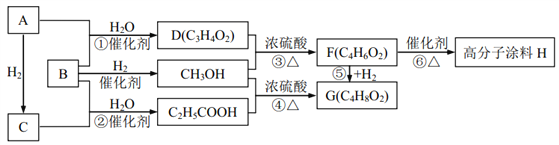
(1)D 中含有的官能团的名称为________________________;
(2)高分子涂料 H 的结构简式为________________________;
(3)下列说法正确的是(___)
A.鉴别有机物 A、 C 可以选用溴的四氯化碳溶液,褪色的是 A
B.反应⑤既是加成反应,又是还原反应,而且原子利用率为 100%
C.高分子涂料 H 含有碳碳双键,所以可以使酸性高锰酸钾溶液褪色
D.反应③④中浓硫酸的作用为催化剂和吸水剂
【答案】 碳碳双键、羧基  BD
BD
【解析】B、C气体在标况下的密度均为1.25g/L;根据M=ρ×Vm=1.25×22.4=28;有机物A与氢气发生加成反应生成分子量为28的有机物乙烯,A为直线结构,为乙炔,根据D得分子式C3H4O2 及反应①原子利用率均为100%,结合B的分子量28,可知B为CO。
(1)从D+CH3OH→C4H6O2,说明D为羧酸,含有一个羧基,再根据分子式C3H4O2可知D的结构简式为CH2=CH-COOH,D 中含有的官能团的名称为碳碳双键、羧基 ;正确答案:碳碳双键、羧基。
(2)D的结构简式为CH2=CH-COOH,与CH3OH发生酯化反应为CH2=CH-COOCH3,(符合分子式C4H6O2),然后在一定条件下发生加聚反应生成高分子涂料, H的结构简式为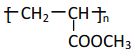 ;正确答案:
;正确答案: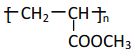 。
。
(3)有机物 A为乙炔,C为乙烯,都含有不饱和键,都能与溴的四氯化碳溶液发生加成反应而使溴水褪色,A错误;CH2=CH-COOCH3+H2→CH3-CH2-COOCH3,该反应既是加成反应,又是还原反应,而且原子利用率为 100%,B正确;高分子涂料H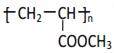 没有碳碳双键,不能被酸性高锰酸钾溶液氧化,C错误;反应③、④均为酯化反应,都需要用到浓硫酸,在反应中起到催化和吸水作用,D正确;正确选项: BD。
没有碳碳双键,不能被酸性高锰酸钾溶液氧化,C错误;反应③、④均为酯化反应,都需要用到浓硫酸,在反应中起到催化和吸水作用,D正确;正确选项: BD。

【题目】下表为元素周期表短同期的一部分, A、B、C、D、E五种元素在周期表中的位置如下图所示。C元素的原子最外层电子数为次外层的3倍。
A | E | C | |
B | D |
回答下列问题:
(1)B元素在周期表中的位置为__________。
(2)D的最高价氧化物对应水化物的化学式为__________。
(3)下列事实能说明C元素的非金属性比硫元素的非金属性强的是__________。
a.C单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1molC单质比1molS得电子多
c.C和S两元素的简单氢化物受热分解,前者的分解温度高
d. C元素的简单氢化物沸点高于S元素的简单氢化物
(4)B与D两元素的单质反应生成化合物M,它的结构类似甲烷,写出M的电子式_____。
(5)A与镁形成的1mol化合物N与水反应,生成2molMg(OH)2和1mol气态烃,该烃分子中碳氢质量比为9:1,写出N与水反应的化学方程式______________________________。
(6)铜与一定浓度的硝酸和硫酸的混合酸反应,生成的盐只有硫酸铜,同时生成的两种气体均由表中两种元素组成,气体的相对分子质量都小于50。为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗1L2.2mol/LNaOH溶液和1molO2,则两种气体的分子式及物质的量分别为__________。