题目内容
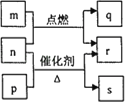
【题目】短周期元素W、X、Y、Z的原子序数依次增大。m、p、q、r、s是由这些元素组成的二元化合物,常温常压下r 为液体,其余均为无色气体。m的摩尔质量为p的2倍,n是元素Y的单质,是绿色植物光合作用产生的无色气体,p物质能使湿润的红色石蕊试纸变蓝,q能使品红溶液褪色。上述转化关系如下图所示。下列说法正确的是( )
A. q与s均为酸性氧化物B. 原子半径:W<Y<X
C. 非金属性:W<Y< XD. Z的含氧酸是一种强酸
【答案】B
【解析】
短周期元素W、X、Y、Z的原子序数依次增加,m、p、q、r、s是由这些元素组成的二元化合物,常温常压下r为液体,则r应为H2O,其余均为无色气体,n是元素Y的单质,是绿色植物光合作用产生的无色气体,则Y为O元素,n为O2,p物质能使湿润的红色石蕊试纸变蓝,则p为NH3,所以W应为H,X应为N元素,根据转化关系,氨气和氧气在催化剂作用下生成r和s,所以s为NO,m的摩尔质量为p的2倍,m应为H2S,q能使品红溶液褪色,则q应为SO2,所以Z应为S元素,硫化氢在氧气中燃烧生成二氧化硫和水,符合转化关系,再结合元素周期律解答。
A. s为NO,为不成盐的氧化物,所以不是酸性氧化物,A项错误;
B. 电子层数越多,原子的半径越大,同周期自左而右原子半径减小,故原子半径H<O<N,即W<Y<X,B项正确;
C.根据元素周期律,同周期元素非金属性从左到右依次增强,同族从上到下元素非金属性依次减弱,则H< N < O,即W < X < Y,C项错误;
D. S元素的含氧酸可以是硫酸,也可以是亚硫酸,其中亚硫酸为弱酸,不是强酸,D项错误;
答案选B。

【题目】2 L密闭容器中进行反应:pZ(g)+qQ(g) ![]() mX(g)+nY(g),式中m、n、p、q为化学计量数。在0~3 min内,各物质的物质的量的变化如下表所示:
mX(g)+nY(g),式中m、n、p、q为化学计量数。在0~3 min内,各物质的物质的量的变化如下表所示:
物质 | X | Y | Z | Q |
起始/mol | 0.7 | 1 | ||
2 min末/mol | 0.8 | 2.7 | 0.8 | 2.7 |
3 min末/mol | 0.8 |
已知:2 min内v(Q)=0.075 mol·L-1·min-1,v(Z)∶v(Y)=1∶2。
请回答下列问题:
(1)2 min内X的反应速率v(X)=__________。
(2)起始时n(Y)=__________。
(3) 3 min末是否达到平衡_______(填是或否)。
(4)对于该反应,能增大正反应速率的措施是________(填序号,下同)。
A.缩小容器体积 B.移走部分Q
C.通入大量He气 D.升高温度
【题目】a、b、c、d是短周期元素,在周期表中的相对位置如图所示.d元素原子核外M层电子数是K层电子数的2倍.下列说法中,错误的是( )
a | b | c |
d |
A. 高温下,a单质可与d的氧化物发生置换反应
B. b的气态氢化物可与其最高价含氧酸反应
C. a、b、c 的最高正化合价等于其所在族序数
D. d的氧化物是制作光导纤维的材料