题目内容
【题目】某化学兴趣小组的同学利用下图所示实验装置进行实验(图中a、b、c表示止水夹)。
![]()
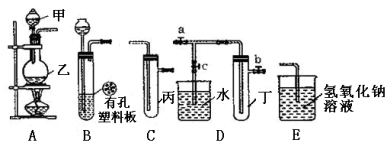
(1)甲、乙两仪器的名称是 、
(2)A、C、E相连后的装置可用于制取Cl2,写出A中发生反应的化学方程式 ,将Cl2通入含有酚酞的NaOH溶液中的现象是 ,该反应的离子方程式为 。
(3)B、D、E装置相连后,在B中盛装浓硝酸和铜片(铜片放在有孔塑料板上),可制得NO2并进行有关实验。
①写出该反应的离子方程式 。
②欲用D装置验证NO2与水的反应,其操作步骤为:先关闭止水夹 ,再打开止水夹 ,使烧杯中的水进入试管丁中。
③试管丁中的NO2与水充分反应后,若向试管内缓缓通入一定量的O2,直至试管全部充满水,则所得溶液中溶质的物质的量浓度是 mol·L1(保留2位有效数值,气体按标准状况计算)。
【答案】(1)分液漏斗、圆底烧瓶(2分)
(2)4HCl(浓)+ MnO2![]() MnCl2 + Cl2↑ + 2H2O (2分)
MnCl2 + Cl2↑ + 2H2O (2分)
溶液红色褪去(1分)Cl2 + 2OH-=Cl- + ClO- + H2O(2分)
(3)①![]() (2分)
(2分)
②a、b ; c (各1分,共2分) ③ 0.045 (2分)
【解析】
试题分析:(1)根据图示仪器的构造特点判断,甲、乙两仪器的名称是分液漏斗、圆底烧瓶。
(2)A、C、E相连后的装置可用于制取Cl2,A中二氧化锰与浓盐酸共热生成二氯化锰、氯气和水,反应的化学方程式为4HCl(浓)+ MnO2![]() MnCl2 + Cl2↑ + 2H2O ,将Cl2通入含有酚酞的NaOH溶液中发生反应:Cl2 + 2OH-==Cl- + ClO- + H2O,溶液红色退去。
MnCl2 + Cl2↑ + 2H2O ,将Cl2通入含有酚酞的NaOH溶液中发生反应:Cl2 + 2OH-==Cl- + ClO- + H2O,溶液红色退去。
(3)①铜与浓硝酸反应生成硝酸铜、二氧化氮和水,该反应的离子方程式为Cu + 2NO3- + 4H+ ==Cu2+ + 2NO2↑+ 2H2O。②欲用D装置验证NO2与水的反应,其操作步骤为:先关闭止水夹a、b,再打开止水夹c,使烧杯中的水进入试管丁中。③试管丁中的NO2与水充分反应后,若向试管内缓缓通入一定量的O2,直至试管全部充满水,直至试管全部充满水,发生反应:4NO2+O2+2H2O==4HNO3,假设试管体积是v,所以溶液体积也是v,二氧化氮体积也是v,所以由公式得:n(NO2)=n(HNO3)=v/22.4 mol ,c(HNO3)=n(HNO3)/v =1/22.4 =0.045 mol/L。

 名校课堂系列答案
名校课堂系列答案【题目】短周期元求X、Y、W在元素周期表中的相对位置如下图所示,其中Z为地壳中含量最高的金属元素。下列说法正确的是
X | ||||||
Y | Z | W |
A.工业上电解YW饱和溶液冶炼金属Y
B.气态氢化物的稳定性:W>X
C.简单离子半径的大小顺序:r(Y+)>r(X-)
D.Y、W的最高价氧化物的水化物均能溶解金厲Z