题目内容
主族元素A、 B、C、D的原子序数都小于18,A与D同主族,B与C在同一周期,A、D原子的最外层电子数都是1,C原子最外层电子数比B原子少2个,且C最外层电子数是次外层电子数的2倍。A、B单质在常温下均为气体,它们在高温下以体积比2∶1完全反应,生成物在常温下是液体。此液体与D单质能激烈反应生成A的单质。所得溶液滴入酚酞显红色,同时溶液中含有与氖原子的电子层结构相同的阳离子。回答下列问题:
B、C、D的原子序数都小于18,A与D同主族,B与C在同一周期,A、D原子的最外层电子数都是1,C原子最外层电子数比B原子少2个,且C最外层电子数是次外层电子数的2倍。A、B单质在常温下均为气体,它们在高温下以体积比2∶1完全反应,生成物在常温下是液体。此液体与D单质能激烈反应生成A的单质。所得溶液滴入酚酞显红色,同时溶液中含有与氖原子的电子层结构相同的阳离子。回答下列问题:
⑴写出元素符号A_ ___,B__ __,C__ __,D_ ___。
⑵写出B与C在高温下完全反应后生成物的化学式______ __,电子式___ __ ,结构式___ ___。
⑶用电子式表示B、D在高温下形成的化合物的电子式_____ _ ___,判断其中的化学键的类型___ __ ___。
⑷写出一种有A、B、C、D组成的化合物的化学式___ ___。
 B、C、D的原子序数都小于18,A与D同主族,B与C在同一周期,A、D原子的最外层电子数都是1,C原子最外层电子数比B原子少2个,且C最外层电子数是次外层电子数的2倍。A、B单质在常温下均为气体,它们在高温下以体积比2∶1完全反应,生成物在常温下是液体。此液体与D单质能激烈反应生成A的单质。所得溶液滴入酚酞显红色,同时溶液中含有与氖原子的电子层结构相同的阳离子。回答下列问题:
B、C、D的原子序数都小于18,A与D同主族,B与C在同一周期,A、D原子的最外层电子数都是1,C原子最外层电子数比B原子少2个,且C最外层电子数是次外层电子数的2倍。A、B单质在常温下均为气体,它们在高温下以体积比2∶1完全反应,生成物在常温下是液体。此液体与D单质能激烈反应生成A的单质。所得溶液滴入酚酞显红色,同时溶液中含有与氖原子的电子层结构相同的阳离子。回答下列问题:⑴写出元素符号A_ ___,B__ __,C__ __,D_ ___。
⑵写出B与C在高温下完全反应后生成物的化学式______ __,电子式___ __ ,结构式___ ___。
⑶用电子式表示B、D在高温下形成的化合物的电子式_____ _ ___,判断其中的化学键的类型___ __ ___。
⑷写出一种有A、B、C、D组成的化合物的化学式___ ___。
A H,B O,C C,D Na。⑵⑶⑷略
略

练习册系列答案
相关题目
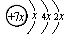 ,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2。
,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2。 ,广泛用于污水处理。
,广泛用于污水处理。 的过程如下:
的过程如下:

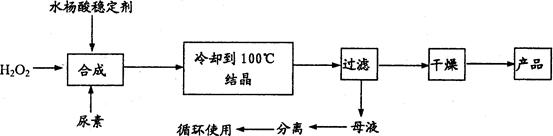
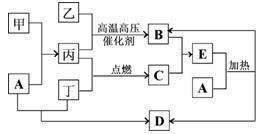
 (碘)、
(碘)、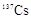 (铯)等。下列说法正确的是( )
(铯)等。下列说法正确的是( ) 与
与 的
的 溶液,pH<13
溶液,pH<13