题目内容
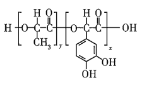
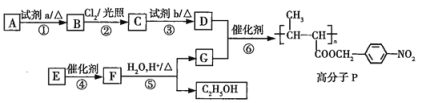
【题目】功能高分子![]() 的合成路线如图所示:
的合成路线如图所示:
(1)![]() 的分子式是
的分子式是![]() ,其结构简式是__________________。
,其结构简式是__________________。
(2)试剂![]() 是__________________。
是__________________。
(3)反应③的化学方程式:__________________。
(4)![]() 的分子式是
的分子式是![]() 。
。![]() 中含有的官能团:__________________。
中含有的官能团:__________________。
(5)反应④的反应类型是__________________。
(6)反应⑤的化学方程式:___________________________。
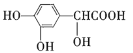
(7)已知:![]() 。以乙烯为起始原料,选用必要的无机试剂合成
。以乙烯为起始原料,选用必要的无机试剂合成![]() ,写出合成路线____________(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
,写出合成路线____________(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
【答案】![]() 浓
浓![]() 和浓
和浓![]()
![]() +NaOH
+NaOH![]()
![]() +NaCl 碳碳双键、酯基 加聚反应
+NaCl 碳碳双键、酯基 加聚反应 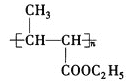 +nH2O
+nH2O![]()
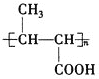 +nC2H5OH
+nC2H5OH ![]()
![]()
【解析】
A的分子式为![]() ,结合高分子P的结构简式推出A为甲苯,B为
,结合高分子P的结构简式推出A为甲苯,B为![]() ,C为
,C为![]() ,D为
,D为![]() ,根据高分子P的结构简式,再结合E的分子式,可推出E的结构简式为CH3CH=CHCOOC2H5,F为
,根据高分子P的结构简式,再结合E的分子式,可推出E的结构简式为CH3CH=CHCOOC2H5,F为 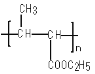 ,G为:
,G为: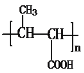 ,据此解答。
,据此解答。
(1)![]() 为甲苯,结构简式为:
为甲苯,结构简式为:![]() ,故答案为:
,故答案为:![]() ;
;
(2)甲苯和浓硝酸在浓硫酸的催化作用下加热发生硝化反应生成![]() ,所以试剂
,所以试剂![]() 为浓硝酸和浓硫酸,故答案为:浓
为浓硝酸和浓硫酸,故答案为:浓![]() 和浓
和浓![]() ;
;
(3)反应③是![]() 在氢氧化钠的水溶液中发生的取代反应,生成对硝基苯甲醇,方程式为:
在氢氧化钠的水溶液中发生的取代反应,生成对硝基苯甲醇,方程式为:![]() +NaOH
+NaOH![]()
![]() +NaCl,故答案为:
+NaCl,故答案为:![]() +NaOH
+NaOH![]()
![]() +NaCl;
+NaCl;
(4)E为![]() ,所含官能团为碳碳双键、酯基,故答案为:碳碳双键、酯基;
,所含官能团为碳碳双键、酯基,故答案为:碳碳双键、酯基;
(5)F是E发生加聚反应生成的高分子化合物,故答案为:加聚反应;
(6)反应⑤为酯的水解反应,方程式为: +nH2O
+nH2O![]()
 +nC2H5OH,故答案为:
+nC2H5OH,故答案为: +nH2O
+nH2O![]()
 +nC2H5OH;
+nC2H5OH;
(7)乙烯和水可以直接加成生成乙醇,乙醇经催化氧化生成乙醛,乙醛发生已知条件中的反应即可以使碳链增长,3-羟基丁醛发生消去反应即可得到2-丁烯醛,2-丁烯醛再被氧化生成2-丁烯酸,该羧酸和乙醇发生酯化反应,即可得到物质E,流程为![]()
![]() ,故答案为:
,故答案为:![]()
![]() 。
。

【题目】某化学实验小组用酸性KMnO4溶液与草酸(H2C2O4)溶液反应,研究外界条件对反应速率的影响,实验操作及现象如下:
编号 | 实验操作 | 实验现象 |
I | 向一支试管中先加入1 mL 0.01 mol/L酸性KMnO4溶液,再加入1滴3 mol/L硫酸和9滴蒸馏水,最后加入1 mL 0.1 mol/L草酸溶液 | 前10 min内溶液紫色无明显变化,后颜色逐渐变浅,30 min后几乎变为无色 |
II | 向另一支试管中先加入1 mL 0.01 mol/L酸性KMnO4溶液,再加入10滴3 mol/L硫酸,最后加入1 mL 0.1 mol/L草酸溶液 | 80 s内溶液紫色无明显变化,后颜色迅速变浅,约150 s后几乎变为无色 |
(1)写出高锰酸钾与草酸反应的离子方程式:______________________________。
(2)由实验I、II可得出的结论是_______________________________。
(3)关于实验II中80 s后溶液颜色迅速变浅的原因,该小组提出猜想:反应中生成的Mn2+对该反应有催化作用。利用提供的试剂设计实验III,验证猜想。提供的试剂:0.01 mol/L酸性 KMnO4溶液,0.1 mol/L草酸溶液,3 mol/L硫酸,MnSO4溶液,MnSO4固体,蒸馏水补全实验III的操作:向试管中先加入1 mL 0.01 mol/L酸性KMnO4溶液,_______,最后加入1 mL 0.1 mol/L草酸溶液。
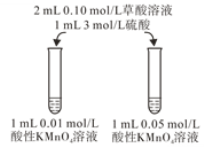
(4)该小组拟采用如图所示的实验方案继续探究KMnO4溶液浓度对反应速率的影响。你认为他们的实验方案______(填“合理”或“不合理”),理由是___________。
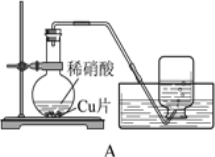
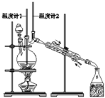
【题目】已知:CH3CH2CH2CH2OH![]() CH3CH2CH2CHO;利用如图装置用正丁醇合成正丁醛相关数据如表:
CH3CH2CH2CHO;利用如图装置用正丁醇合成正丁醛相关数据如表:
物质 | 沸点/℃ | 密度 / gcm-3 | 水中溶解性 |
|
正丁醇 | 117.2 | 0.8109 | 微溶 | |
正丁醛 | 75.7 | 0.8017 | 微溶 |
下列说法中,不正确的是
A.为防止产物进一步氧化,应将酸化的Na2Cr2O7溶液逐滴加入正丁醇中
B.当温度计1示数为90~95℃,温度计2示数在76℃左右时,收集产物
C.反应结束,将馏出物倒入分液漏斗中,分去水层,粗正丁醛从分液漏斗上口倒出
D.向获得的粗正丁醛中加入少量金属钠,检验其中是否含有正丁醇