题目内容
(每空2分,共14分)某河道两旁有甲乙两厂。它们排放的工业废水中,共含K+、Ag+、Fe3+、C1-、OH- 、NO3- 六种离子。
甲厂的废水明显呈碱性,故甲厂废水中所含的三种离子是_____________。乙厂的废水中含有另外三种离子。对于该两厂的废水,可采取下列两种方法来处理。
(1)如果在废水中加一定量 (选填:活性炭或铁粉),可以发生反应,离子方程式是 ,并且能够回收其中的金属 (填写金属元素符号)。
(2)将甲厂和乙厂的废水按适当的比例混合,可以使废水中的某些离子转化为沉淀,写出两个离子方程式: ; 。经过滤后的废水主要含 ,可用来浇灌农田。
【答案】
( 每空2分,共14分)
OH-、C1-、K+;
(1)铁粉、Fe+2Ag+=2Ag+Fe2+;Ag
(2)Ag++C1-=AgC1↓ 、Fe3++3OH-=Fe(OH)3↓; KNO3
【解析】甲厂的废水明显呈碱性,因此Fe3+、Ag+肯定在乙厂,而C1-与Ag+不能共存,因此C1-肯定在甲厂,再根据溶液呈电中性知K+肯定在甲厂,NO3-肯定在乙厂。
⑴根据题意废水中加一定量铁粉可以如下发生反应:Fe+2Fe3+=3Fe2+、Fe+2Ag+=2Ag+Fe2+
⑵由题意,反应为Ag++C1-=AgC1↓ 、Fe3++3OH-=Fe(OH)3↓,剩下的是KNO3、。

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
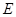 可以发生反应:2E+I
可以发生反应:2E+I 2F+D,F中的E元素的质量分数为60%.
2F+D,F中的E元素的质量分数为60%.