题目内容
5.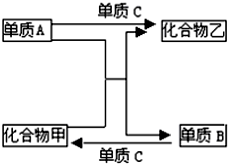 A、B、C是三种短周期元素的单质,甲、乙是两种常见的化合物.这些化合物和单质之间存在如下图所示的关系.据此判断:
A、B、C是三种短周期元素的单质,甲、乙是两种常见的化合物.这些化合物和单质之间存在如下图所示的关系.据此判断:(1)在甲、乙两种化合物中,不含有组成A元素的化合物是甲(填“甲”或“乙”).
(2)单质A、B可能是同主族的非金属吗?可能(填“可能”或“不可能”),若可能,写出符合反应“单质A+化合物甲=单质B+化合物乙”的化学方程式:(若填“可能”,则应写出准确方程式才能给分,下同)2C+SiO2$\frac{\underline{\;高温\;}}{\;}$ Si+2CO;
(3)单质A、B可能是同周期的金属吗?可能(填“可能”或“不可能”),若可能,写出符合反应“单质A+化合物甲=单质B+化合物乙”的化学方程式:Zn+CuCl2=ZnCl2+Cu;
(4)单质A是金属、单质B是非金属,可能吗?可能(填“可能”或“不可能”),若可能,写出符合反应“单质A+化合物甲=单质B+化合物乙”的化学方程式:2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$ 2MgO+C.
分析 A、B、C是三种常见元素的单质,甲、乙是两种常见的化合物,甲+A=B+乙是置换反应,A+C=乙是化合反应,B+Z=甲是化合反应,A可能是氢气或者碳或者活泼金属,A和C会生成乙,B和C会生成甲,金属和酸生成盐和氢气,所以A是氢气或碳或镁等进行分析,A可以是金属,如为Al,Mg等,Al+HCl→AlCl3+H2,Z为Cl2;Mg+CO2→C+MgO,Z为O2;Al+Fe2O3→Al2O3+Fe,Z为O2;A、B、C可以全部为非金属单质,如:C+SiO2→Si+CO,Z为O2;若A、B为金属单质,是金属间的置换反应,所以化合物一定是金属的非金属化合物,所以Z必为非金属单质;若A、B为非金属单质,则Z不一定是金属单质,可以是非金属单质,如:C+SiO2→Si+CO,Z为O2 ;
解答 解:(1)分析可知:甲+A=B+乙是置换反应,A+Z=乙是化合反应,B+Z=甲是化合反应,所以不含A元素的化合物为甲,
故答案为:甲;
(2)单质A、B可能是同主族的非金属,第ⅣA主族中碳还原二氧化硅,符合单质A+化合物甲=单质B+化合物乙”的反应,反应的化学方程式为:2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO,
故答案为:可能,2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO;
(3)单质A、B可能是同周期的金属,如第四周期的锌和铜之间可以发生置换反应,反应的化学方程式:Zn+CuCl2=ZnCl2+Cu,
故答案为:可能,Zn+CuCl2=ZnCl2+Cu;
(4)单质A是金属、单质B是非金属,可以发生置换反应,如镁和二氧化碳反应生成碳和氧化镁,反应的化学方程式为:2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C,
故答案为:可能,2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C.
点评 本题考查了物质转化关系的综合应用,主要考查置换反应的分析应用,反应特征的应用,熟练掌握物质性质和置换反应的类型是解题关键,题目难度中等.

| 酸 | 电离方程式 | 电离平衡常数Ka |
| CH3COOH | CH3COOH?═?CH3COO-+H+ | 1.76×10-5 |
| H2CO3 | H2CO3???H++HCO3- HCO3-???H++CO32- | Ka1=4.31×10-7 Ka2=5.61×10-11 |
| H3PO4 | H3PO4???H++H2PO4- H2PO4-??H++HPO42- HPO42-??H++PO43- | Ka1=7.52×10-3 Ka2=6.23×10-8 Ka3=4.50×10-13 |
| A. | 温度升高,K值减小 | |
| B. | 0.1 mol/L CH3COOH溶液中加入少量冰醋酸,c(H+)/c(CH3COOH)值将增大 | |
| C. | 等物质的量浓度的各溶液pH关系为:pH(Na2CO3)>pH(CH3COONa)>pH(Na3PO4) | |
| D. | PO43-、HPO42-和H2PO4-在溶中不能大量共存 |
( )
| A. | 溶液中Na+浓度不变,有氧气生成 | |
| B. | 溶液中OH-浓度增大,有氢气放出 | |
| C. | 溶液中OH-浓度不变,溶液总质量增大 | |
| D. | 溶液中Na+数目减少,溶液总质量减少 |
| A. | AlCl3 | B. | NH4HCO3 | C. | KHCO3 | D. | Fe2 (SO4)3 |
| A. | X与W可以形成W2X、W2X2两种化合物 | |
| B. | Y元素最高价氧化物对应水化物的化学式为H2YO4 | |
| C. | Z元素的非金属性比X元素的非金属性强 | |
| D. | Y、Z两元素的简单离子的半径Y>Z |
①CH3CH2CH2CH2CH3
②CH3CH2CH2OH
③CH3CH2CH3
④CH3CHBrCH3
⑤(CH3)2-CH-CH=CH-CH3
⑥

⑦CH2OH-CHOH-CH2OH
⑧(CH3)2-CH-COOH
⑨CH3CH2CH2CHO
请你按要求对以上有机化合物进行分类,并把正确答案的序号填入下表中:
| 烷烃 | 烯烃 | 芳香烃 | 卤代烃 | 醇 | 醛 | 羧酸 | 脂肪烃 |
| ①③ | ⑤ | ⑥ | ④ | ②⑦ | ⑨ | ⑧ | ①③⑤ |

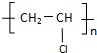 ;
; .
. .
.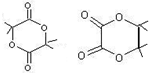 (写出一个即可).
(写出一个即可).