题目内容
【题目】运用化学反应原理研究化学反应有着非常重要的意义。
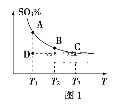
(一)硫酸生产中,SO2催化氧化生成SO3:2SO2(g)+O2(g)![]() 2SO3(g),混合体系中SO3的百分含量和温度的关系如图1所示(曲线上任何一点都表示平衡状态)。
2SO3(g),混合体系中SO3的百分含量和温度的关系如图1所示(曲线上任何一点都表示平衡状态)。
①2SO2(g)+O2(g)![]() 2SO3(g)的ΔH___0(填“>”或“<”);若在恒温、恒压条件下向上述平衡体系中通入氦气,平衡___移动(填“向左”“向右”或“不”)。
2SO3(g)的ΔH___0(填“>”或“<”);若在恒温、恒压条件下向上述平衡体系中通入氦气,平衡___移动(填“向左”“向右”或“不”)。
②若反应进行到状态D时,v(正)___v(逆)(填“>”“<”或“=”)。
(二)工业上合成氨技术叫哈伯法:N2(g)+3H2(g)![]() 2NH3(g) ΔH<0,此法达到平衡时反应物的转化率不高。
2NH3(g) ΔH<0,此法达到平衡时反应物的转化率不高。
①能使该反应的反应速率增大,且平衡向正反应方向移动的措施是___(填编号)。
A.使用更高效的催化剂
B.升高温度
C.及时分离出氨气
D.充入氮气,增大氮气的浓度(保持容器体积不变)
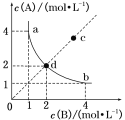
②若在某温度下,2L的密闭容器中发生合成氨的反应,图2表示N2的物质的量随时间的变化曲线。用H2表示0~10min内该反应的平均速率v(H2)=__。

从11min起,压缩容器的体积为1L,则n(N2)的变化曲线为___(填编号)。
A.a B.b C.c D.d
【答案】< 左 > D 0.06mol·L-1·min-1 D
【解析】
(一)①根据图像,可以判断出该反应是放热反应,则ΔH<0;若在恒温、恒压条件下向上述平衡体系中通入氦气,容器的体积增大,相当于恒容减小压强,则平衡向左移动;
(二)①根据平衡移动的速率图像分析即可;
②通过N2的反应速率来计算H2的反应速率,再通过平衡的移动来分析N2物质的量的变化趋势。
(一)①由图知,随着温度升高,体系中SO3的百分含量降低,说明平衡逆向移动,则该反应的正反应是放热反应,故ΔH<0;若在恒温、恒压条件下向上述平衡体系中通入氦气,容器的体积增大,相当于恒容减小压强,平衡向气体体积增大的方向进行,即平衡向左移动;
②T1℃时,D点的SO3的百分含量比A点(平衡时)低,则平衡向SO3的百分含量增大的方向进行,即平衡正向移动,故v(正)>v(逆);
(二)①A、使用催化剂,反应速率增大,但是平衡不移动,A错误;
B、该反应是放热反应,升高温度,反应速率增大,但是平衡逆向移动,B错误;
C、及时分离出氨气,降低了生成物的浓度,平衡正向移动,但是也会降低反应速率,C错误;
D、增大氮气的浓度,可加快反应速率,且平衡正向移动,D正确;
故选D;
②v(N2)=![]() =0.02mol·L-1·min-1,v(H2)=3v(N2)=3×0.02mol·L-1·min-1=0.06mol·L-1·min-1;从11min起,压缩容器体积,则体系压强增大,平衡正向移动,N2的浓度减小,故选D。
=0.02mol·L-1·min-1,v(H2)=3v(N2)=3×0.02mol·L-1·min-1=0.06mol·L-1·min-1;从11min起,压缩容器体积,则体系压强增大,平衡正向移动,N2的浓度减小,故选D。