题目内容
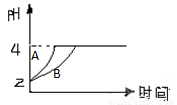
(8分)常温下,取0.1 mol/L HA溶液与0.1 mol/L NaOH溶液等体积混合(混合后溶液体积的变化不计),测得混合溶液的pH=8。试回答以下问题:
(1)混合后溶液的pH=8的原因是____________________________(用离子方程式表示)。
(2)混合后的溶液中由水电离出的c(OH-)____0.1 mol/L NaOH溶液中由水电离出的c(OH-) (填“>”、“<”或“=”)。
(3)已知NH4A溶液为中性,又知将HA溶液加到NaHCO3溶液中有气体放出,试推断NH4HCO3溶液的pH________7(填“>”、“<”或“=”)。
(4)有相同温度下相同浓度的四种盐溶液:A.NH4HCO3;B.NH4A;C.(NH4)2SO4;D.NH4Cl,按pH由大到小的顺序排列________(填序号)。
【答案】
(1)A-+H2O HA+OH- (2)> (3)> (4) ABDC
HA+OH- (2)> (3)> (4) ABDC
【解析】略

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
小学课时特训系列答案
相关题目
Ⅰ.配平下列反应方程式:
NaIO3+ NaHSO3-- I2+ Na2SO4+ H2SO4+ H2O
Ⅱ.废旧金属的回收再利用是保护自然资源的有力措施.一批成分不详的合金废料,为了确定其成分和再利用途径,探究性学习小组拟定以下方案进行实验分析:
请回答下列问题:
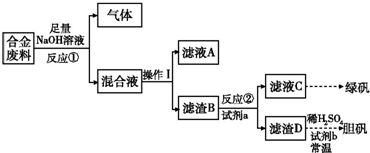
(1)从上述信息知,该合金中可确定的成分有 ;(填化学式)
(2)滤渣D中加入稀硫酸和试剂b,常温下可制得胆矾,是一种绿色化学工艺,则试剂b是 ;写出总反应方程式 ;
(3)甲、乙两同学都验证了反应①生成气体是氢气,甲同学推断滤液A应是NaAlO2;乙同学查阅资料得知硅与NaOH溶液反应也有H2放出,因此持不同意见,请你设计一最佳方案,帮助他们作一确证:(写出选用试剂、实验判断现象及得出结论)
(4)取质量均为m g的滤渣B四份,分别加入同浓度,不同体积的稀HNO3充分反应,在标准状况生成NO(设还原产物只有一种)体积与剩余固体金属的质量如下表:
①实验1溶解的金属是 ;质量为 g;
②写出实验4中金属恰好溶解后,发生反应的离子方程式: .实验4中V的数值为 .
Ⅱ.废旧金属的回收再利用是保护自然资源的有力措施.一批成分不详的合金废料,为了确定其成分和再利用途径,探究性学习小组拟定以下方案进行实验分析:
请回答下列问题:

(1)从上述信息知,该合金中可确定的成分有
(2)滤渣D中加入稀硫酸和试剂b,常温下可制得胆矾,是一种绿色化学工艺,则试剂b是
(3)甲、乙两同学都验证了反应①生成气体是氢气,甲同学推断滤液A应是NaAlO2;乙同学查阅资料得知硅与NaOH溶液反应也有H2放出,因此持不同意见,请你设计一最佳方案,帮助他们作一确证:(写出选用试剂、实验判断现象及得出结论)
(4)取质量均为m g的滤渣B四份,分别加入同浓度,不同体积的稀HNO3充分反应,在标准状况生成NO(设还原产物只有一种)体积与剩余固体金属的质量如下表:
| 实验编号 | 1 | 2 | 3 | 4 |
| 稀HNO3体积(mL) | 100 | 200 | 300 | 400 |
| 剩余金属质量(g) | 9.0 | 4.8 | 0 | 0 |
| NO体积(L) | 1.12 | 2.24 | 3.36 | V |
②写出实验4中金属恰好溶解后,发生反应的离子方程式:
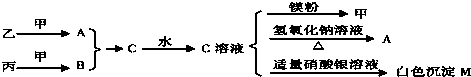
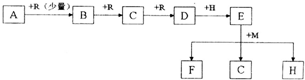
 4C(g)
4C(g) 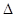 H
>0 达到平衡时,c(A)=2mol/L,
c(B)=7mol/L, c(C)=4mol/L。试确定B的起始浓度c(B)的取值范围是
;若改变条件重新达到平衡后体系中C的体积分数增大,下列措施可行的是
H
>0 达到平衡时,c(A)=2mol/L,
c(B)=7mol/L, c(C)=4mol/L。试确定B的起始浓度c(B)的取值范围是
;若改变条件重新达到平衡后体系中C的体积分数增大,下列措施可行的是