题目内容
3.设NA为阿伏伽德罗常数的值.下列说法正确的是( )| A. | 0.1 mol.L-1NaCl溶液中Na+的数目为0.1NA | |
| B. | 标准状况下,11.2 L H2O中含有分子的数目为0.5NA | |
| C. | 常温常压下,14g由N2与CO组成的混合气体含有的原子数目为NA | |
| D. | 1 mol Na被完全氧化生成Na2O2,失去个电子数为2NA |
分析 A、溶液体积不明确;
B、标况下,水为液态;
C、氮气和CO的摩尔质量均为28g/mol;
D、根据反应后钠元素变为+1价来分析.
解答 解:A、溶液体积不明确,故溶液中的钠离子的个数无法计算,故A错误;
B、标况下,水为液态,故不能根据气体摩尔体积来计算其物质的量,故B错误;
C、氮气和CO的摩尔质量均为28g/mol,故14g混合物的物质的量n=$\frac{14g}{28g/mol}$=0.5mol,而氮气和CO均为双原子分子,故0.5mol混合气体中含1mol原子即NA个,故C正确;
D、反应后钠元素变为+1价,故1mol钠失去1mol电子即NA个,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案
相关题目
13.X、Y、Z三种元素的原子,其核外电子排布分别为:X原子最外层有一个电子,Y原子的第一、二、三层电子数分别为2、8、3,Z原子第一、二层电子数为2、6,由这三种元素组成的化合物的化学式可能是( )
| A. | XYZ2 | B. | XYZ3 | C. | X2YZ2 | D. | X2YZ3 |
11.下列反应中,反应后固体物质没有增重的是( )
| A. | 碳酸钡粉末加入到足量稀硫酸中 | B. | Na2O2粉末空气中露置一段时间 | ||
| C. | 铝与足量V2O5发生铝热反应 | D. | 将足量铁屑投入CuCl2溶液 |
18.NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 标准状况下,2.24 L Cl2通入足量NaOH溶液中,反应转移电子的数目为0.2NA | |
| B. | 1 mol K与足量O2反应,生成K2O、K2O2和KO2的混合物时转移的电子数为NA | |
| C. | 常温常压下,1.7 g H2O2中含有的电子数为NA | |
| D. | 标准状况下,1 mol CO2所含共用电子对数为2NA |
8.同周期的X,Y和Z三种元素,已知关系如下:HXO4,H2YO4和H3ZO4的酸性依次减弱,下列判断不正确的是( )
| A. | 非金属性:X最强,Z最弱 | |
| B. | 原子半径:X最大,Z最小 | |
| C. | 气态氢化物稳定性:HX最强 | |
| D. | 气态氢化物水溶液酸性:ZH3<H2Y<HX |
15.下列说法中,错误的是( )
| A. | 二氧化碳可用于灭火 | |
| B. | 可用pH试纸测定溶液酸碱度 | |
| C. | 可用灼烧的方法鉴定羊毛、合成纤维 | |
| D. | 稀释浓硫酸时可将水倒入盛有浓硫酸的烧杯中 |
13.氨甲环酸和氨甲苯酸是临床上常用的止血药,其结构如图.下列说法正确的是( )
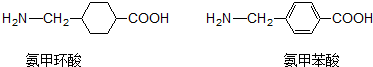
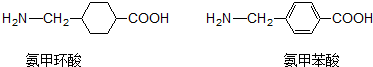
| A. | 氨甲环酸、氨甲苯酸都能发生取代、氧化、加聚、加成等反应 | |
| B. | 氨甲环酸、氨甲苯酸中都有5种不同的氢原子 | |
| C. | 氨甲环酸与氨甲苯酸互为同分异构体 | |
| D. | 氨甲环酸、氨甲苯酸都能与NaOH溶液反应 |