��Ŀ����
����Ŀ������ʮ�����Ǿ��иߴ����ܶȵ��������壬������ʮ������C10H18������������C10H12��������C10H8��������������ͷ���������֪��
C10H18(l)![]() C10H12(l)��3H2(g) ��H1
C10H12(l)��3H2(g) ��H1
C10H12(l)![]() C10H8(l)��2H2(g) ��H2
C10H8(l)��2H2(g) ��H2
��H1����H2��0��C10H18��C10H12�Ļ��ΪEa1��C10H12��C10H8�Ļ��ΪEa2��ʮ�����ij�ѹ�е�Ϊ192������192����Һ̬ʮ���������ⷴӦ��ƽ��ת����ԼΪ9������ش�
��1�����������������Ӧƽ��ת���ʵ�������_________��
A�����¸�ѹ B�����µ�ѹ C�����µ�ѹ D�����¸�ѹ
��2���о���������������ʮ�������ں����ܱշ�Ӧ���У������¶ȴ�����ѹ����������Ҳ���������⣬������______________________________________________________��
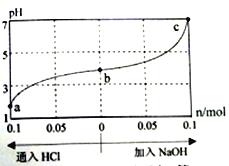
��3���¶�335�����ں����ܱշ�Ӧ���н��и�ѹҺ̬ʮ������1.00 mol��������ʵ�飬���C10H12��C10H8�IJ���x1��x2�������ʵ��������ƣ���ʱ��仯��ϵ����ͼ1��ʾ��


����8 hʱ����Ӧ��ϵ����������Ϊ__________mol��������������Ӧ����
��x1��������x2��ԭ����________________________________________��
����ͼ2�л�����C10H18��C10H12��C10H8��������������Ӧ������ʾ��ͼ��
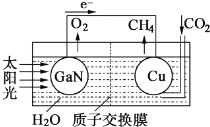
������ѧ�ҷ��֣���H2O��N2Ϊԭ�ϣ�����NaOH��KOHΪ����ʣ�����Fe2O3����������250���ͳ�ѹ�¿�ʵ�ֵ绯ѧ�ϳɰ��������������ı仯����Ϊ���������У��벹��������
��4���缫��Ӧʽ��________________________________��2Fe��3H2O��N2��Fe2O3��2NH3��
���𰸡� C ��Ӧ���ȣ��¶����ߣ�ƽ�������ƶ������ͬʱ���¶����ߵ���ʮ����������Ũ������ƽ�������ƶ��������������������� ��1.951���ڷ�Ӧ2�Ļ�ܱȷ�Ӧ1С����ͬ�¶��·�Ӧ2���죬������ͬʱ���ڣ����ɵ��������ֶ�ת��Ϊ������x1��������x2.  Fe2O3+6e-+3H2O=2Fe+6OH
Fe2O3+6e-+3H2O=2Fe+6OH
������������(1)C10H18(l)![]() C10H12(l)��3H2(g) ��H1��C10H12(l)
C10H12(l)��3H2(g) ��H1��C10H12(l)![]() C10H8(l)��2H2(g) ��H2����H1����H2��0����Ϊ���ȷ�Ӧ���Ҷ�������������ʵ�������ķ�Ӧ��
C10H8(l)��2H2(g) ��H2����H1����H2��0����Ϊ���ȷ�Ӧ���Ҷ�������������ʵ�������ķ�Ӧ��
A�������¶ȣ�ƽ�������ƶ���ƽ��ת������������ѹǿ��ƽ�������ƶ���ƽ��ת���ʼ�С����A����B�������¶ȣ�ƽ�������ƶ���ƽ��ת���ʼ�С����B����C�������¶ȣ�ƽ�������ƶ���ƽ��ת��������Сѹǿ��ƽ�������ƶ���ƽ��ת��������C��ȷ��D�������¶ȣ�ƽ�������ƶ���ƽ��ת���ʼ�С����D����ѡC��
(2)�ܷ�ӦΪ�÷�ӦΪ���ȷ�Ӧ�������¶ȣ�ƽ�������ƶ���ƽ��ת��������ƽ�ⳣ�������¶ȴﵽ192��ʱ��ʮ����������Ũ������ƽ�������ƶ��������������������ӣ��ʴ�Ϊ����Ӧ���ȣ��¶����ߣ�ƽ�������ƶ������ͬʱ���¶����ߵ���ʮ����������Ũ������ƽ�������ƶ��������������������ӣ�
(3)���¶�335�棬��8 hʱ��ʮ����Ϊ1.00 mol�����C10H12��C10H8�IJ���x1=0.027��x2=0.374��������C10H12��C10H8�����ʵ����ֱ�Ϊ0.027mol��0.374mol���跴Ӧ��C10H18�����ʵ���Ϊa����ӦC10H12�����ʵ���Ϊb�����ݷ�Ӧ
C10H18(l)![]() C10H12(l)��3H2(g)
C10H12(l)��3H2(g)
1 1 3
a a 3a
C10H12(l)![]() C10H8(l)��2H2(g)��
C10H8(l)��2H2(g)��
1 1 2
b b 2b
��a-b=0.027��b=0.374����a=0.401��������ɵ����������ʵ�������Ϊ3a+2b=3��0.401+2��0.374=1.951������������Ϊ1.951mol���ʴ�Ϊ��1.951��
�ڷ�Ӧ2�Ļ�ܱȷ�Ӧ1С����ͬ�¶��·�Ӧ2���죬������ͬʱ���ڣ����ɵ��������ֶ�ת��Ϊ������x1��������x2���ʴ�Ϊ����Ӧ2�Ļ�ܱȷ�Ӧ1С����ͬ�¶��·�Ӧ2���죬������ͬʱ���ڣ����ɵ��������ֶ�ת��Ϊ������x1��������x2��
��C10H18(l)![]() C10H12(l)��3H2(g) ��H1��C10H12(l)
C10H12(l)��3H2(g) ��H1��C10H12(l)![]() C10H8(l)��2H2(g) ��H2����H1����H2��0��������Ӧ��Ϊ���ȷ�Ӧ������������������ڷ�Ӧ���C10H18��C10H12��C10H8��������������Ӧ������ ʾ��ͼΪ
C10H8(l)��2H2(g) ��H2����H1����H2��0��������Ӧ��Ϊ���ȷ�Ӧ������������������ڷ�Ӧ���C10H18��C10H12��C10H8��������������Ӧ������ ʾ��ͼΪ ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
����(4)��H2O��N2Ϊԭ�ϣ�����NaOH��KOHΪ����ʣ�����Fe2O3����������250��ͳ�ѹ�¿�ʵ�ֵ绯ѧ�ϳɰ���������������ԭ��Ӧ����������һ����Ӧ2Fe��3H2O��N2��Fe2O3��2NH3����֪��Fe2O3������������ת��Ϊ������˵缫��ӦʽΪFe2O3+6e-+3H2O=2Fe+6OH-���ʴ�Ϊ��Fe2O3+6e-+3H2O=2Fe+6OH-��