题目内容
下列物质在溶于水和熔化时,破坏的作用力完全相同的是( )
| A、干冰 |
| B、冰醋酸 |
| C、NaHSO4 |
| D、KOH |
考点:不同晶体的结构微粒及微粒间作用力的区别
专题:化学键与晶体结构
分析:根据物质的构成判断物质的晶体类型,不同类型的晶体的作用力不同,以此解答该题.
解答:
解:A、干冰属于分子晶体溶于水生成碳酸会电离,所以破坏了分子间作用力和共价键,干冰熔化破坏分子间作用力,故A不选;
B、冰醋酸属于分子晶体,溶于水发生电离,破坏了分子间作用力和共价键,熔化破坏分子间作用力,故B不选;
C、NaHSO4属于离子晶体溶于水发生电离,破坏了离子键和共价键,熔化破坏离子键,故C不选;
D、KOH属于离子晶体,溶于水和熔化均破坏离子键,故D选;
故选D.
B、冰醋酸属于分子晶体,溶于水发生电离,破坏了分子间作用力和共价键,熔化破坏分子间作用力,故B不选;
C、NaHSO4属于离子晶体溶于水发生电离,破坏了离子键和共价键,熔化破坏离子键,故C不选;
D、KOH属于离子晶体,溶于水和熔化均破坏离子键,故D选;
故选D.
点评:本题考查了化学键和晶体类型的判断,根据晶体中存在的化学键及晶体的构成微粒确定晶体类型,根据微粒之间的作用力判断化学键,题目难度不大.

练习册系列答案
相关题目
下列物质在一定条件下,不能和氢气发生加成反应的是( )
| A、乙醛 | B、丙酮 | C、乙酸 | D、甲苯 |
下列关于乙烯和聚乙烯的叙述不正确的是( )
| A、乙烯常温下是气体,为纯净物;聚乙烯常温下是固体,为混合物 |
| B、乙烯的化学性质比聚乙烯活泼 |
| C、取等质量的乙烯和聚乙烯完全燃烧后,生成的CO2和H2O的质量分别相等 |
| D、乙烯和聚乙烯都能使酸性高锰酸钾溶液褪色 |
下列化学用语书写正确的是( )
A、氯原子的结构示意图: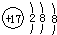 |
B、CO2的比例模型: |
C、氯化氢的电子式: |
| D、二氧化硅分子式:SiO2 |
关于离子键和离子化合物的说法中,正确的是( )
| A、阴阳离子之间通过静电吸引形成离子键 |
| B、阴阳离子之间通过离子键一定能形成离子化合物 |
| C、离子化合物一定能导电 |
| D、只有在活泼金属元素与活泼非金属元素化合时,才能形成离子键 |
W粒子的结构示意图如图所示,下列关于它的说法不正确的是( )
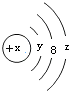

| A、y=2 |
| B、若x=18,则z=8 |
| C、若x=14,则其氢化物的化学式为H2W |
| D、若x=17,则其最高价氧化物的化学式为W2O7 |
某溶液中含有HCO3-、SO32-、Cl-和Na+,若向其中通入足量的Cl2,溶液中上述四种离子的浓度基本保持不变的是( )
| A、HCO3- |
| B、SO32- |
| C、Cl- |
| D、Na+ |
下列表示物质结构的化学用语正确的是( )
| A、HT、D2互为同素异形体 |
B、HF的电子式: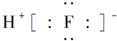 |
C、NH4Cl的电子式: |
D、CaC2的电子式: |