题目内容
某溶液中含有HCO3-、SO32-、Cl-和Na+,若向其中通入足量的Cl2,溶液中上述四种离子的浓度基本保持不变的是( )
| A、HCO3- |
| B、SO32- |
| C、Cl- |
| D、Na+ |
考点:离子反应发生的条件
专题:离子反应专题
分析:氯气具有强氧化性,能氧化具有还原性的物质,氯气和水反应生成盐酸,盐酸是强酸,能和碳酸氢根离子反应生成二氧化碳.
解答:
解:向含有HCO3-、SO32-、Cl-和Na+的溶液中通入氯气,
发生的离子反应有:Cl2+H2O=H++Cl-+HClO、Cl2+SO32-+H2O=2H++2Cl-+SO42-、H++HCO3-=CO2+H2O,
所以离子的浓度基本保持不变的是钠离子,
故选D.
发生的离子反应有:Cl2+H2O=H++Cl-+HClO、Cl2+SO32-+H2O=2H++2Cl-+SO42-、H++HCO3-=CO2+H2O,
所以离子的浓度基本保持不变的是钠离子,
故选D.
点评:本题以氯气的性质为载体考查了离子反应,明确离子之间发生的反应是解本题关键,难度不大.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
有关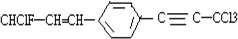 分子结构的叙述中,正确的是( )
分子结构的叙述中,正确的是( )
 分子结构的叙述中,正确的是( )
分子结构的叙述中,正确的是( )| A、除苯环以外的其余碳原子有可能都在一条直线上 |
| B、除苯环以外的其余碳原子在一条直线上 |
| C、12个碳原子不可能都在同一平面上 |
| D、12个碳原子有可能都在同一平面上 |
下列物质在溶于水和熔化时,破坏的作用力完全相同的是( )
| A、干冰 |
| B、冰醋酸 |
| C、NaHSO4 |
| D、KOH |
共价键、离子键和范德华力都是微观粒子之间的不同作用力,下列物质:①NaOH;②SiO2;③碘;④金刚石;⑤NaCl;⑥干冰,其中含有两种作用力的组合是( )
| A、①②⑤ | B、①③⑥ |
| C、②④⑥ | D、①②③⑥ |
下列溶液中,一定能大量共存的离子组是( )
| A、能使氢氧化铝迅速溶解的溶液:Na+、Fe2+、NO3-、SO42- |
| B、能使酚酞试液变红的溶液:Na+、NH4+、CO32-、SO42- |
| C、含有大量SO42-的透明溶液:K+、Cu2+、Cl-、NO3- |
| D、含有大量ClO-的溶液:H+、Mg2+、I-、SO42- |
下列离子方程式书写正确的是( )
| A、在氯化亚铁溶液中加入稀硝酸:3Fe2++4H++NO3-═3Fe3++2H2O+NO↑ |
| B、NaHCO3溶液与盐酸的反应:CO32-+2H+═H2O+CO2↑ |
| C、用FeCl3溶液腐蚀铜线路板:Cu+Fe3+═Cu2++Fe2+ |
| D、AlCl3溶液中加入过量氨水:Al3++4OH-═AlO2-+2H2O |
下列文字表述与反应方程式对应且正确的是:( )
| A、溴乙烷中滴入AgNO3溶液检验其中的溴元素:Br-+Ag+═AgBr↓ | ||
B、乙醇与溴水溶液反应:C2H5OH+HBr
| ||
C、甲苯与浓硝酸和浓硫酸的混合物反应: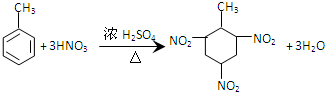 | ||
D、实验室用液溴和苯制溴苯: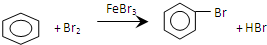 |
下列物质进行一氯取代反应后,只能生成四种沸点不同产物的烃是( )
| A、(CH3)2CHCH2CH2CH3 |
| B、(CH3CH2)2CHCH3 |
| C、(CH3)2CHCH(CH3)2 |
| D、(CH3)3CCH2CH3 |
己烯雌酚是一种激素类药物,结构如下,下列有关叙述中不正确的是( )


| A、可与NaOH和NaHCO3发生反应 |
| B、1mol该有机物可以与7mol H2发生反应 |
| C、可以用有机溶剂萃取 |
| D、1mol该有机物可以与5mol Br2发生反应 |