题目内容
【题目】(1)2 mol O3和3 mol O2的质量之比_____,分子数之比____,同温同压的密度之比为____,含氧原子数之比为________,体积之比为________。
(2)气体化合物A分子式可表示为OxFy,已知同温同压下10 mL A受热分解生成15 mL O2和10 mL F2,则A的化学式为________,推断的依据为________________和_________________ 定律。
【答案】1:1 2:3 3:2 1:1 2:3 O3F2 阿伏加德罗定律 质量守恒定律
【解析】
(1)氧气和臭氧都是氧原子构成的不同单质,根据m=nM计算O3和O2的质量之比;根据阿伏加德罗定律可知,二者的分子数之比等于物质的量之比;在相同条件下,气体的密度之比是摩尔质量之比;根据N=nNA计算含有的氧原子数之比;根据阿伏加德罗定律可知,二者的体积之比等于物质的量是之比.
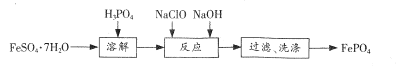
(2)根据质量守恒定律和阿伏加德罗定律,写出分解方程式为2OxFy![]() 3O2+2F2,则可推断化学式。
3O2+2F2,则可推断化学式。
(1)氧气和臭氧都是氧原子构成的不同单质,所以2 molO3和3 mol O2的质量之比1:1;根据阿伏加德罗定律可知,二者的分子数之比是2:3;在相同条件下,气体的密度之比是摩尔质量之比,因此二者的密度之比是48:32=3:2;由化学式可知,含有的氧原子数之比是1:1;根据阿伏加德罗定律可知,二者的体积之比是2:3。
故答案为:1:1;2:3;3:2;1:1;2:3.
(2)根据质量守恒定律和阿伏加德罗定律,写出分解方程式为2OxFy![]() 3O2+2F2,则A化学式为O3F2,故答案为:O3F2;阿伏加德罗定律和质量守恒定律.
3O2+2F2,则A化学式为O3F2,故答案为:O3F2;阿伏加德罗定律和质量守恒定律.

【题目】Bodensteins研究反应H2(g)+I2(g)![]() 2HI(g),温度为T时,在两个体积均为1 L的密闭容器中进行实验,测得气体混合物中碘化氢的物质的量分数w (HI)与反应时间t的关系如下表:
2HI(g),温度为T时,在两个体积均为1 L的密闭容器中进行实验,测得气体混合物中碘化氢的物质的量分数w (HI)与反应时间t的关系如下表:
容器编号 | 起始物质 | t/min | 0 | 20 | 40 | 60 | 80 | 100 |
I | 0.5 mol I2、0.5 mol H2 | w (HI)/% | 0 | 50 | 68 | 76 | 80 | 80 |
II | x mol HI | w (HI)/% | 100 | 91 | 84 | 81 | 80 | 80 |
研究发现上述反应中:v正=ka·w(H2)·w(I2),v逆=kb·w2(HI),其中ka、kb为常数。下列说法正确的是:
A. 温度为T时,该反应![]() = 64
= 64
B. 容器I中在前20 min的平均速率v(HI)=0.0125 mol·L-1·min-1
C. 若起始时向容器I中加入物质的量均为0.1 mol的H2、I2、HI,反应逆向进行
D. 若两容器中存在kaⅠ=kaⅡ且kbⅠ=kbⅡ,则x的值一定为1