题目内容
14.硫代硫酸钠是一种重要的化工产品.工业上常利用含硫废水生产Na2S2O3•5H2O,实验室可用如下装置(略去部分加持仪器)模拟生成过程.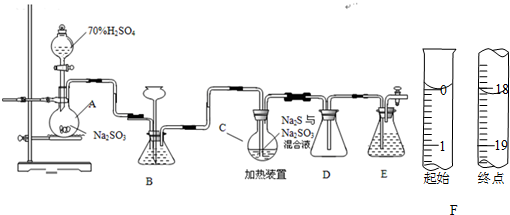
烧瓶C中发生反应如下:
Na2S(aq)+H2O(l)+SO2(g)=Na2SO3(aq)+H2S(aq) (I)
2H2S(aq)+SO2(g)=3S(s)+2H2O(l) (Ⅱ)
S(s)+Na2SO3(aq)$\frac{\underline{\;\;△\;\;}}{\;}$Na2S2O3(aq) (Ⅲ)
(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液注,若液柱高度保持不变,则整个装置气密性良好.装置D的作用是防止倒吸.装置E中为NaOH溶液.
(2)为提高产品纯度,应使烧瓶C中Na2S和Na2SO3恰好完全反应,则烧瓶C中Na2S和Na2SO3物质的量之比为2:1.
(3)装置B的作用之一是观察SO2的生成速率,其中的液体最好选择c.
a.蒸馏水 b.饱和Na2SO3溶液c.饱和NaHSO3溶液 d.饱和NaHCO3溶液
(4)实验中,为使SO2缓慢进入烧瓶C,采用的操作是控制滴加硫酸的速度.
(5)已知反应(Ⅲ)相对较慢,则烧瓶C中反应达到终点的现象是溶液变澄清(或浑浊消失).
(6)反应终止后,烧瓶C中的溶液经蒸发浓缩冷却,过滤,洗涤,干燥,即得到粗产品(主要含有Na2S2O3•5H2O和其他杂质).某兴趣小组为测定该产品纯度,准确称取4.96 g产品,用适量蒸馏水溶解,以淀粉作指示剂,用0.1000 mol•L?1碘的标准溶液滴定.反应原理为:2S2O32-+I2=S4O62-+2I?,滴定至终点时,滴定起始和终点的液面位置如图,则产品的纯度为18.1%.经仪器分析,该产品纯度为16%,分析该兴趣小组测定产品纯度偏差的原因(忽略人为误差)粗产品中含有Na2SO3(或Na2S)可以消耗I2,使消耗的碘水体积偏大.[M(Na2S2O3•5H2O)=248g/mol].
分析 (1)液柱高度保持不变,说明气密性良好;D中左侧为短导管,为安全瓶,防止倒吸;装置E起到吸收尾气中SO2、H2S的作用;
(2)根据题目所给3个反应,可得出对应关系:2Na2S~2H2S~3S~3 Na2SO3,2Na2S反应时同时生成2Na2SO3,还需要1Na2SO3;
(3)观察SO2的生成速率,则二氧化硫通过溶液不能与SO2反应,有气泡逸出;
(4)通过分液漏斗的活塞控制滴加硫酸的速度,可以控制产生二氧化硫的速率;
(5)根据C中发生的反应可知,烧瓶C中反应达到终点发生的反应为硫与亚硫酸钠反应生成硫代硫酸钠;
(6)根据图示的滴定管中液面读出初读数、终读数,然后计算出消耗碘的标准溶液体积,根据反应2S2O32-+I2═S4O62-+2I-可知,n(S2O32-)=2n(I2),然后碘单质的物质的量计算出Na2S2O3•5H2O质量及产品的纯度;产品纯度测量值偏大,粗产品中含有Na2SO3(或Na2S)可以消耗I2,使消耗的碘水体积偏大.
解答 解:(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液柱,若液柱高度保持不变,则气密性良好;D中左侧为短导管,为安全瓶,防止倒吸;装置E起到吸收尾气中SO2、H2S的作用,可选用NaOH溶液,
故答案为:液柱高度保持不变;防止倒吸;NaOH;
(2)装置A中反应的化学方程式为:Na2SO3+H2SO4═Na2SO4+SO2↑+H2O,根据题目所给3个反应,可得出对应关系:2Na2S~2H2S~3S~3Na2SO3,2Na2S反应时同时生成2Na2SO3,还需要1Na2SO3,所以烧瓶C中Na2S和Na2SO3物质的量之比为2:1,
故答案为:2:1;
(3)观察SO2的生成速率,是通过观察溶液中产生气泡的快慢来判断,所以溶液不能与SO2反应,选项中只有饱和NaHSO3溶液与二氧化硫不反应,
故答案为:c;
(4)分液漏斗有玻璃活塞,通过控制分液漏斗的活塞控制滴加硫酸的速度,可以控制产生二氧化硫的速率,所以为使SO2缓慢进入烧瓶C,采用的操作是控制滴加硫酸的速度,
故答案为:控制滴加硫酸的速度;
(5)根据C中发生的反应可知,烧瓶C中反应达到终点发生反应为硫与亚硫酸钠反应生成硫代硫酸钠,反应的现象为溶液变澄清(或混浊消失),
故答案为:溶液变澄清(或浑浊消失);
(6)根据图示的滴定管中液面可知,滴定管中初始读数为0.00mL,滴定终点液面读数为18.10mL,所以消耗碘的标准溶液体积为18.10mL-0.00mL=18.10mL;
根据反应2S2O32-+I2═S4O62-+2I-可知,n(S2O32-)=2n(I2),所以4.96g产品中含有Na2S2O3•5H2O质量为:0.1000 mol•L-1×18.10×10-3L×2×248g/mol=0.89776g,故则产品的纯度为:$\frac{0.89776g}{4.96g}$×100%=18.1%,经仪器分析,该产品纯度为16%,产品纯度测量值偏大,粗产品中含有Na2SO3(或Na2S)可以消耗I2,使消耗的碘水体积偏大,
故答案为:18.1%;粗产品中含有Na2SO3(或Na2S)可以消耗I2,使消耗的碘水体积偏大.
点评 本题考查实验方案的分析与评价,涉及气密性检验、离子检验、对操作的分析评价、化学计算等,侧重实验分析能力及知识综合应用能力的考查,(2)为易错点,也可以利用总反应的分析,题目难度中等.

 名校课堂系列答案
名校课堂系列答案| A. | AlCl3 | B. | Na2O2 | C. | FeCl2 | D. | Al2S3 |
| A. | 饱和氯水中Cl-、NO3-、Na+、SO32- | B. | 在碱性溶液中CO32-、K+、SO42-、Br- | ||
| C. | Na2S溶液中SO42-、K+、Cl-、Cu2+ | D. | pH=12的溶液中NO3-、I-、Na+、Al3+ |
| 实验编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |
| n(X) | n(Y) | n(M) | ||
| ① | 700 | 0.40 | 0.10 | 0.090 |
| ② | 800 | 0.10 | 0.40 | 0.080 |
| ③ | 800 | 0.20 | 0.30 | a |
| ④ | 900 | 0.10 | 0.15 | b |
| A. | 实验①中,若5min 时测得 n(M)=0.050 mol,则0至5 min时间内,用N表示的平均反应速率v(N)=1.0×10-2 mol/min | |
| B. | 实验②中,该反应的平衡常数K=2.0 | |
| C. | 实验③中,达到平衡时,X的转化率为60% | |
| D. | 实验④中,达到平衡时,b>0.060 |
( )
| A. | (3)(7)(9)(10)(11)(12) | B. | (3)(7)(9)(10)(11)(14) | C. | (3)(7)(8)(9)(10)(11)(12) | D. | (1)(3)(7)(8)(9)(10)(11)(12) |
| 选项 | 化学反应及其离子方程式 | 评 价 |
| A | NaHSO4溶液与Ba(OH)2溶液反应至 SO42-沉淀完全: 2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O | 正 确 |
| B | 向碳酸镁溶液中加入足量稀盐酸: CO32-+2H+=CO2↑+H2O | 错误,碳酸镁不应写成离子形式 |
| C | 向沸水中滴加饱和的氯化铁溶液至液体变为红褐色: Fe3++3H2O=Fe(OH)3↓+3H+ | 正 确 |
| D | NaOH溶液中通入少量CO2反应:OH-+CO2=HCO3- | 正 确 |
| A. | A | B. | B | C. | C | D. | D |
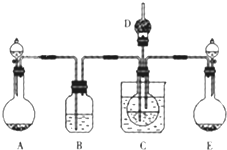

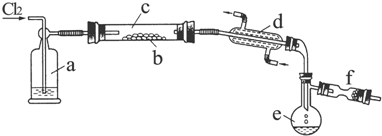
 .
.