题目内容
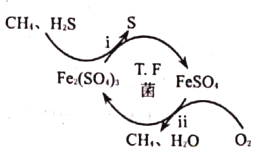
【题目】硫化氢是危害性极强的毒性气体,也是恶臭气体的主要成分之一。![]() 菌在酸性溶液中可实现天然气的催化脱硫,其原理如图所示。下列说法正确的是( )
菌在酸性溶液中可实现天然气的催化脱硫,其原理如图所示。下列说法正确的是( )
A.![]() 在脱硫过程中被还原
在脱硫过程中被还原
B.温度越高,越有利于天然气的催化脱硫
C.该脱硫过程需要不断添加![]() 溶液
溶液
D.理论上,需要氧气的体积是相同状态下![]() 体积的一半
体积的一半
【答案】D
【解析】
A.由图可知,![]() 在过程中转化为
在过程中转化为![]() ,化合价升高,作还原剂,被氧化,A 错误;
,化合价升高,作还原剂,被氧化,A 错误;
B.温度过高, 细菌会失去活性,不利于催化脱硫, B 错误;
C.图中硫酸铁为催化剂,催化剂在反应前后的质量和性质保持不变,不需要不断添加, C 错误;
D.该过程实质为![]() 与
与![]() 反应生成
反应生成![]() 和
和![]() 方程式为:2H2S+O2=2H2O+2S;故理论上消耗
方程式为:2H2S+O2=2H2O+2S;故理论上消耗![]() 的物质的量是
的物质的量是![]() 的一半,D 正确;
的一半,D 正确;
故答案为:D。

【题目】POCl3常用作半导体掺杂剂及光导纤维原料,实验室制备POCl3并测定产品含量的实验过程如下:
I.实验室制备POCl3。
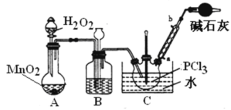
采用氧气氧化液态PCl3法制取POCl3,实验装置(加热及夹持仪器略)如图:
资料:① Ag+ + SCN- =AgSCN↓,Ksp(AgCl) >Ksp(AgSCN);
②PCl3和POCl3的相关信息如下表:
物质 | 熔点/℃ | 沸点/℃ | 相对分子质量 | 其他 |
PCl3 | -112.0 | 76.0 | 137.5 | 两者互溶,均为无色液体,遇水均剧烈反应生成含氧酸和氯化氢 |
POCl3 | 2.0 | 106.0 | 153.5 |
(1)PCl3分子中各原子均满足8电子稳定结构,则PCl3的电子式为____。
(2)B中所盛的试剂是____,干燥管的作用是________。
(3)POCl3遇水反应的化学方程式为_____________。
(4)反应温度要控制在60~65℃,原因是:__________。
II.工业上可用氯化水解法生产三氯氧磷,工艺流程如下:
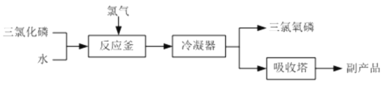
(5)氯化水解法生产三氯氧磷的化学方程式为____。
(6)通过佛尔哈德法可以测定三氯氧磷产品中Cl元素含量,实验步骤如下:
a、准确称取30.7 g POCl3产品,置于盛有60.00 mL蒸馏水的水解瓶中摇动至完全水解,将水解液配成100.00mL溶液。
b、取10. 00 mL溶液于锥形瓶中,加入10.00 mL 3.2 mol·L-1 AgNO3标准溶液。
c、加入少许硝基苯用力摇动,使沉淀表面被有机物覆盖。
d、以X为指示剂,用0.2 mol·L-1 NH4SCN溶液滴定过量的AgNO3溶液,达到滴定终点时共用去l0.00 mL NH4SCN溶液。
①步骤c中加入硝基苯的作用是____。
②步骤d中X为______。
A FeCl2 B NH4Fe(SO4)2 C 淀粉 D 甲基橙
③三氯氧磷产品中Cl元素的质量百分含量为____。