题目内容
6.将铂电极放置在KOH溶液中,然后分别向两极通入CH4和O2,即产生电流,称为甲烷燃料电池.已知甲烷燃料电池两个电极上的反应分别为:CH4-8e-+10OH-=CO32-+7H2O
2O2+8e-+4H2O=8OH-
下列有关说法中错误的是( )
| A. | CH4在负极上反应;O2在正极上反应 | B. | 放电过程中电解质溶液的碱性减弱 | ||
| C. | 此电池属于环境友好电池 | D. | 此电池中化学能100%转化为电能 |
分析 甲烷燃料电池中,负极上燃料失电子发生氧化反应,电极反应为CH4-8e-+10OH-═CO32-+7H2O,正极上通入氧化剂,电极反应为2O2+8e-+4H2O═8OH-,反应过程中氢氧根离子参加反应,导致溶液中氢氧根离子浓度减小,据此分析解答.
解答 解:A.甲烷燃料电池中,燃料失电子发生氧化反应,所以CH4在负极上反应,O2在正极上反应,故A正确;
B.根据CH4+2O2+2OH-═CO32-+3H2O知,氢氧根离子参加反应,所以溶液中氢氧根离子浓度降低,溶液的碱性减弱,故B正确;
C.该电池放电时不产生对环境有污染的物质,所以属于环境友好电池,故C正确;
D.化学能主要转化为电能,还转化为热能,故D错误;
故选D.
点评 本题考查了化学电源新型电池,根据得失电子确定正负极上通入的物质及发生的反应,难点是电极反应式的书写,要结合溶液酸碱性书写,为易错点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
16.下列有关化学键的说法中,不正确的是( )
| A. | 氢键不是化学键,而是一种特殊的分子间作用力 | |
| B. | 化学键可以使离子相结合,也可以使原子相结合 | |
| C. | 化学反应过程中,反应物分子的化学键断裂消耗能量,生成物分子中化学键形成放出能量 | |
| D. | 氯化钠中存在离子键,所以食盐水是离子化合物 |
14.下列有关电化学原理的说法中,错误的是( )
| A. | 在现实生活中,电化学腐蚀要比化学腐蚀严重的多,危害更大 | |
| B. | 在铜的精炼装置中,通常用粗铜作作阴极,精铜作阳极 | |
| C. | 氯碱工业,主要依托电解熔融的氯化钠来制取工业上重要的化工原料烧碱和氯气 | |
| D. | 可充电的电池称“二次电池”,在充电时,是将电能转变成化学能,在放电时,又将化学能转化成电能 |
1.${\;}_{27}^{60}$Co是γ放射源,${\;}_{27}^{60}$Co可用于农作物的诱变育种,我国用该方法培育出了许多农作物新品种.对${\;}_{27}^{60}$Co原子的叙述正确的是( )
| A. | 质量数是27 | B. | 质子数是60 | C. | 中子数是27 | D. | 质子数是27 |
3.下列反应中氯元素仅被还原的是( )
| A. | 5Cl2+I2+6H2O═10HCl+2HIO3 | |
| B. | 2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O | |
| C. | MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+2H2O+Cl2↑ | |
| D. | HCl+NaOH═NaCl+H2O |
4.常温下可以盛放浓硫酸的容器是( )
| A. | 塑料 | B. | Fe | C. | Al | D. | Mg |

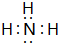 ;
; 短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中,T所处的周期序数与主族序数相等.请回答下列问题:
短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中,T所处的周期序数与主族序数相等.请回答下列问题: .
.