题目内容
9.A和B是前三周期的元素,它们的离子A2+和B3+具有相同的核外电子层结构,下列说法正确的是( )| A. | 原子半径:A>B | B. | 原子序数:A>B | ||
| C. | 离子半径:A2+<B3+ | D. | 质量数:A>B |
分析 A和B是短周期的两种元素,离子A2+和B3+具有相同的核外电子层结构,则A、B位于同一周期,A在第IIA族,B在第IIIA族,同周期从左到右原子半径减小,据此解答.
解答 解:A和B是短周期的两种元素,离子A2+和B3+具有相同的核外电子层结构,则A、B位于同一周期,A在第IIA族,B在第IIIA族,
A.同周期从左到右原子半径减小,则原子半径:A>B,故A正确;
B.同周期从左到右原子原子序数增大,则原子序数:A<B,故B错误;
C.电子层结构相同核电荷数越大离子半径越小,故离子半径A2+>B3+,故C错误;
D.一般原子序数越大,质量数越大,则质量数:A<B,故D错误.
故选A.
点评 本题考查结构与位置关系、元素周期律等,确定元素在周期表中的位置是关键,难度不大.

练习册系列答案
相关题目
4.下列水溶液中的电离方程式书写不正确的是( )
| A. | H2O+H2O?H3O++OH- | B. | NaHSO4═Na++HSO4- | ||
| C. | NaHS═Na++HS- | D. | HCO3-+H2O?H3O++CO32- |
20.25℃时,浓度均为为0.1mol/L的HA溶液和BOH溶液,pH分别是1和11,下列说法正确的( )
| A. | BOH溶于水,其电离方程式是BOH═B++OH- | |
| B. | 若将一定量的上述溶液混合后pH=7,则c(A- )=c(B+) | |
| C. | 在0.1mol/L BA溶液中,c(B+)>c(A- )>c(OH- )>c(H+) | |
| D. | 若将0.1mol/L BOH溶液稀释至0.001mol/L,则溶液的pH=9 |
17.下列离子方程式正确的是( )
| A. | 乙酸与碳酸钠溶液反应:2H++CO${\;}_{3}^{2-}$═CO2↑+H2O | |
| B. | 醋酸溶液与新制氢氧化铜反应:CH3COOH+OH-→CH3COO-+H2O | |
| C. | 甲醛溶液与足量的银氨溶液共热:HCHO+4[Ag(NH3)2]++4OH-$\stackrel{△}{→}$ CO${\;}_{3}^{2-}$+2NH${\;}_{4}^{+}$+4Ag↓+6NH3+2H2O | |
| D. | 苯酚钠溶液中通入少量二氧化碳:C6H5O-+CO2+H2O→C6H5OH+CO32- |
14.在SO2+2H2S═3S+2H2O反应中,还原剂的是( )
| A. | SO2 | B. | H2S | C. | S | D. | H2O |
19.如图所示装置中,a、b都是惰性电极,通电一段时间后,b电极附近溶液呈红色.下列说法正确的是( )
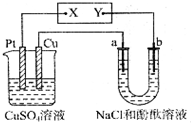

| A. | X是负极,Y是正极 | B. | Pt是阴极,Cu是阳极 | ||
| C. | CuSO4溶液的pH逐渐减小 | D. | CuSO4溶液的pH不变 |
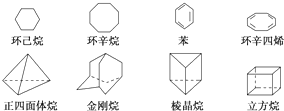
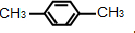 1,4-二甲苯;
1,4-二甲苯; 1,3,5-三甲苯.
1,3,5-三甲苯.