题目内容
【题目】(1)Cu的一种氯化物晶胞结构如图所示(黑球表示铜原子,白球表示氯原子),该氯化物的化学式是__。若该晶体的密度为ρg·cm-3,以NA表示阿伏加德罗常数的值,则该晶胞的边长a=__nm。

(2)一种四方结构的超导化合物的晶胞如图1所示,晶胞中Sm和As原子的投影位置如图2所示。

图中F-和O2-共同占据晶胞的上下底面位置,若两者的比例依次用x和1x代表,则该化合物的化学式表示为__,通过测定密度ρ和晶胞参数,可以计算该物质的x值,完成它们关系表达式:ρ=__g·cm-3。
以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图1中原子1的坐标为(![]() ,
,![]() ,
,![]() ),则原子2和3的坐标分别为__、__。
),则原子2和3的坐标分别为__、__。
【答案】CuCl  SmFeAsO1-xFx
SmFeAsO1-xFx 
![]()
![]()
【解析】
(1)该晶胞中Cu位于顶点和面心,个数为![]() ,Cl位于体内,个数为4,该氯化物的化学式为CuCl;设该晶胞的边长为a nm,则有
,Cl位于体内,个数为4,该氯化物的化学式为CuCl;设该晶胞的边长为a nm,则有![]() ,解得a=
,解得a= ;故答案为:CuCl;
;故答案为:CuCl; ;
;
(2)由晶胞结构中各原子所在位置可知,该晶胞中Sm个数为![]() ,Fe的个数为
,Fe的个数为![]() ,As的个数为
,As的个数为![]() ,O或者F的个数为
,O或者F的个数为![]() ,即该晶胞中O和F的个数和为2,F—的比例为x,O2—的比例为1-x,故该化合物的化学时为SmFeAsO1-xFx,1个晶胞的质量为
,即该晶胞中O和F的个数和为2,F—的比例为x,O2—的比例为1-x,故该化合物的化学时为SmFeAsO1-xFx,1个晶胞的质量为 ,1个晶胞的体积为a2c pm3=a2c×10-30cm3,则密度
,1个晶胞的体积为a2c pm3=a2c×10-30cm3,则密度 ;原子2位于底面的中心,即z轴坐标为0,其分数坐标为
;原子2位于底面的中心,即z轴坐标为0,其分数坐标为![]() ;原子3位于z轴上,其分数坐标为
;原子3位于z轴上,其分数坐标为![]() ,故答案为: SmFeAsO1-xFx;
,故答案为: SmFeAsO1-xFx; ;
;![]() ;
;![]() 。
。

【题目】含碳化合物种类繁多。回答下列问题:
(1)一定温度下,在密闭容器中将等物质的量的CO(g)和H2O(g)混合,采用适当的催化剂进行反应CO(g)+H2O(g)![]() CO2(g)+H2(g),已知此温度下,该反应的平衡常数K=16,则平衡时体系中H2的物质的量分数为_________%。
CO2(g)+H2(g),已知此温度下,该反应的平衡常数K=16,则平衡时体系中H2的物质的量分数为_________%。
(2)在催化剂Ru催化下,CO2与H2反应可生成CH4,反应方程式为CO2(g)+4H2(g)![]() CH4(g)+2H2O(g)。已知H2的体积分数随温度的升高而增加。若温度从300℃升至400℃,重新达到平衡,则v正______(填“增大”“减小”或“不变”,下同),v逆_______,平衡常数K________,转化率α________;若在相同温度时,上述反应在不同起始浓度下分别达到平衡,各物质的平衡浓度如下表:
CH4(g)+2H2O(g)。已知H2的体积分数随温度的升高而增加。若温度从300℃升至400℃,重新达到平衡,则v正______(填“增大”“减小”或“不变”,下同),v逆_______,平衡常数K________,转化率α________;若在相同温度时,上述反应在不同起始浓度下分别达到平衡,各物质的平衡浓度如下表:
c(CO2)/mol/L | c(H2)/mol/L | c(CH4)/mol/L | c(H2O)/mol/L | |
平衡I | a | b | c | d |
平衡II | m | n | x | y |
则a、b、c、d与m、n、x、y之间的关系式为_____________。
(3)已知相关物质的电离平衡常数如下表:
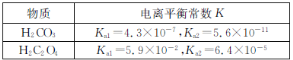
①0.1 mol·L-1的Na2CO3溶液的pH_______(填“大于”“小于”或“等于”)0.1 mol·L-1的Na2C2O4溶液的pH。
②若将等浓度的草酸溶液和碳酸溶液等体积混合,溶液中粒子浓度大小的顺序正确的是_________(填字母)。
a.c(H+)>c(HC2O4-)>c(HCO3-)>c(CO32-) b.c(HCO3-)>c(HC2O4-)>c(C2O42-)>c(CO32-)
c.c(H+)>c(HC2O4-)>c(CO32-)>c(C2O42-) d.c(H2CO3)>c(HCO3-)>c(HC2O4-)>c(CO32-)
【题目】1,2-二氯丙烷(CH2ClCHClCH3)是一种重要的化工原料,工业上可用丙烯加成法制备,主要副产物为3-氯丙烯(CH2=CHCH2Cl),反应原理为:
I.CH2=CHCH3(g)+Cl2(g) ![]() CH2ClCHClCH3(g) H1=-134kJ·mol-1
CH2ClCHClCH3(g) H1=-134kJ·mol-1
II.CH2=CHCH3(g)+Cl2(g) CH2=CHCH2Cl(g)+HCl(g) H2=-102kJ·mol-1
请回答下列问题:
(1)已知CH2=CHCH2Cl(g)+HCl(g) ![]() CH2ClCHClCH3(g)的活化能Ea(正)为132kJ·mol-1,则该反应的活化能Ea(逆)为___________kJ·mol-1。
CH2ClCHClCH3(g)的活化能Ea(正)为132kJ·mol-1,则该反应的活化能Ea(逆)为___________kJ·mol-1。
(2)一定温度下,密闭容器中发生反应I和反应II,达到平衡后增大压强,CH2ClCHClCH3的产率____________(填“增大”“减小”或“不变”),理由是_________________________________。
(3)起始时向某恒容绝热容器中充入1 mol CH2=CHCH3和1 mol Cl2发生反应II,达到平衡时,容器内气体压强_________________(填“增大”“减小”或“不变”)。
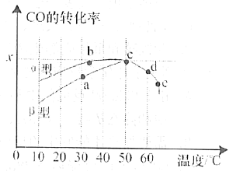
(4)某研究小组向密闭容器中充入一定量的CH2=CHCH3和Cl2,分别在A、B两种不同催化剂作用下发生反应,一段时间后测得CH2ClCHClCH3的产率与温度的关系如图所示。p点是否为对应温度下CH2ClCHClCH3的平衡产率,_________填“是”或“否”)判断理由是_______________________。
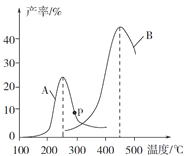
(5)一定温度下,向恒容密闭容器中充入等物质的量的CH2=CHCH3(g)和Cl2(g)。在催化剂作用下发生反应I,容器内气体的压强随时间的变化如下表所示。
时间/min | 0 | 60 | 120 | 180 | 240 | 300 | 360 |
压强/kPa | 80 | 74.2 | 69.4 | 65.2 | 61.6 | 57.6 | 57.6 |
①用单位时间内气体分压的变化来表示反应速率,即![]()
②该温度下,若平衡时HCl的体积分数为![]() ,则丙烯的平衡总转化率
,则丙烯的平衡总转化率![]() ____________;反应I的平衡常数Kp=____________________kPa-1(Kp为以分压表示的平衡常数,保留小数点后2位)。
____________;反应I的平衡常数Kp=____________________kPa-1(Kp为以分压表示的平衡常数,保留小数点后2位)。