题目内容
【题目】对H2O2的分解速率影响因素进行研究。在相同温度下,实验测得不同条件下出O2浓度随时间变化如图所示。下列说法不正确的是( )
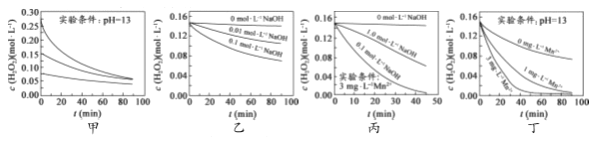
A. 图甲表明,可通过适当增大H2O2浓度,加快H2O2分解速率
B. 图乙表明,可通过调节溶液的酸碱性,控制H2O2分解速率快慢
C. 图丙表明,Mn2+少量存在时,碱性太强,不利于H2O2分解
D. 图乙、图丙和图丁表明,Mn2+是H2O2分解的催化剂,提高Mn2+的浓度就能增大H2O2 分解速率
【答案】D
【解析】A.图甲中溶液的pH相同,但浓度不同,浓度越大,相同时间内浓度的变化量越大,由此得出相同pH条件下,双氧水浓度越大,双氧水分解速率越快,故A正确;B.图乙中H2O2浓度相同,但加入NaOH浓度不同,说明溶液的pH不同,NaOH浓度越大,相同时间内双氧水浓度变化量越大,由此得出:双氧水浓度相同时,pH越大双氧水分解速率越快,故B正确;C.图丙中少量Mn2+存在时,相同时间内双氧水浓度变化量:0.1mol/LNaOH溶液>1.0mol/LNaOH溶液>0mol/LNaOH溶液,由此得出:锰离子作催化剂时受溶液pH的影响,但与溶液的pH值不成正比,碱性太强,不利于H2O2分解,故C正确;D.图丁中pH相同,锰离子浓度越大,相同时间内双氧水浓度变化量越大,但图丙中锰离子作催化剂时受溶液pH的影响,碱性太强,不利于H2O2分解,故D错误;故选D。

练习册系列答案
相关题目