题目内容
【题目】已知:
P4(白磷,s)+5O2(g)═P4O10(s)△H=﹣2983.2kJ/mol
P(红磷,s)+ ![]() O2(g)═
O2(g)═ ![]() P4O10(s)△H=﹣738.5kJ/mol
P4O10(s)△H=﹣738.5kJ/mol
试写出白磷转化为红磷的热化学方程式;白磷的稳定性比红磷(填“高”或“低”).
【答案】P4(白磷,s)=4 P(红磷,s)△H=﹣29.2 kJ/mol;低
【解析】解:P4(s,白磷)+5O2(g)=P4O10(s)△H1=﹣2983.2kJ/mol…①
P(s,红磷)+ ![]() O2(g)=
O2(g)= ![]() P4O10(s)△H2=﹣738.5kJ/mol…②
P4O10(s)△H2=﹣738.5kJ/mol…②
根据盖斯定律:①﹣②×4可得:P4(s,白磷)=4P(s,红磷)△H=(﹣2983.2kJ/mol)﹣(﹣738.5kJ)×4=﹣29.2kJ/mol,
说明白磷转化为红磷是放热反应,相同的状况下,能量比白磷低,而能量越低,物质越稳定,故白磷稳定性低于红磷,
所以答案是:P4(白磷,s)=4 P(红磷,s)△H=﹣29.2 kJ/mol;低.

【题目】甲醇是主要的化学工业基础原料和清洁液体燃料.工业上可以用CO或CO2来生产燃料甲醇.已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:
化学反应及平衡常数 | 温度/℃ | ||
500 | 800 | ||
①2H2(g)+CO(g)CH3OH(g)△H1 | K1 | 2.5 | 0.15 |
②H2(g)+CO2(g)CO(g)+H2O(g)△H2 | K2 | 1.0 | 2.50 |
③3H2(g)+CO2(g)CH3OH(g)+H2O(g)△H3 | K3 | ||
(1)反应②的反应热△H20(填“>”、“<”或“=”);
(2)某温度下反应①中H2的平衡转化率(a)与体系总压强(P)的关系如图1所示.则平衡状态由A变到B时,平衡常数K(A)K(B) (填“>”、“<”或“=”);
(3)根据反应①与②可推导出K1、K2与K3之间的关系,则K3=(用K1、K2表示).500℃时测得反应③在某时刻H2(g)、CO2(g)、CH3OH(g)、H2O(g)的浓度(mol/L)分别为0.8、0.1、0.3、0.15,则此时v(正)v(逆) (填“>”、“<”或“=”);
(4)在3L容积可变的密闭容器中发生反应②,已知c(CO)与反应时间t变化曲线Ⅰ如图2所示,若在t0时刻分别改变一个条件,曲线Ⅰ变为曲线Ⅱ和曲线Ⅲ.当曲线Ⅰ变为曲线Ⅱ时,改变的条件是;当曲线Ⅰ变为曲线Ⅲ时,改变的条件是; 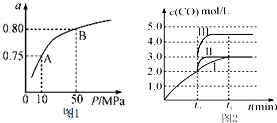
(5)一定条件下甲醇与一氧化碳反应可以合成乙酸.通常状况下,将amol/L的乙酸与bmol/LBa(OH)2溶液等体积混合,反应平衡时,2c(Ba2+)=c(CH3COO﹣),用含a和b的代数式表示该混合溶液中乙酸的电离常数为 .