��Ŀ����
��10�֣�����Ҫ��ش��������⡣
��1���������ģ�Ϳ�����������ʶ�л���Ľṹ��
������ij�л���ķ��ӱ���ģ�ͣ����в�ͬ��ɫ���������ͬ��ԭ�ӣ���֮��ġ�����
��ʾ������˫����������
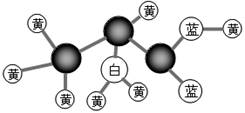
���л�������п��ܴ��ڵ����ֹ����ŵ����Ʒֱ�Ϊ �� �� �� ��
�����л����ڻ�ѧ�����ϱ��ֵ��ص��� �� ��
��2���л�����������ʳ��������л���֮��ļ���
�������������Ǻ͵��ۣ���ѡ�� �� ������ĸ����
A����ˮ B��������Һ C������ D��NaOH��Һ
�������� ��
��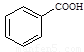 ����ѡ�� �� (����ĸ)��
����ѡ�� �� (����ĸ)��
A��AgNO3��Һ B��NaOH��Һ C��FeCl3��Һ D��Na2CO3��Һ
��3��ͬ���칹�������л���������ԭ��֮һ��
����ʽΪC7H6O2���л����ж���ͬ���칹�壬���к��б�����1��������ͬ���칹��Ľṹ��ʽ�� �� �� �� ������
��4���߷��ӻ����������������������Ź㷺��Ӧ�á�
PES���۶������Ҷ���������һ������ɽ���ľ������������ϱ�Ĥ��ʳƷ��װ�ȷ������Ź㷺��Ӧ�á���ṹ��ʽ���£�
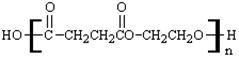
�ϳ�PES���л���ѧ��Ӧ������ �� ��Ӧ���γɸþۺ�������ֵ���Ľṹ��ʽ�ֱ��� �� �� �� ��
(10��)
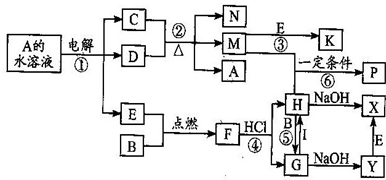
��1���������Ȼ� ������
��2����AB ��CD
��3�� ��
��
��4������ HOOCCH2CH2COOH HOCH2CH2OH ��ÿ��1�֣�
��������

 ÿ��10���ӿ�����������������ϵ�д�
ÿ��10���ӿ�����������������ϵ�д�