题目内容
【题目】三聚氰酸的结构如图所示,下列有关三聚氰酸的说法不正确的是( ) 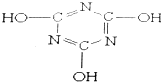
A.分子式为C3H3N3O3
B.属于共价化合物
C.分子中只含极性键,不含非极性键
D.该分子中的C原子采取sp3杂化
【答案】D
【解析】解:A.由结构可知分子式为C3H3N3O3 , 故A正确;B.只含共价键,为共价化合物,故B正确;
C.O﹣H、C﹣N、C=N、C﹣O均为极性键,故C正确;
D.C原子形成2个单键和1个双键,分子中的C原子采取sp2杂化,故D错误;
故选D.
【考点精析】本题主要考查了有机物的结构和性质的相关知识点,需要掌握有机物的性质特点:难溶于水,易溶于汽油、酒精、苯等有机溶剂;多为非电解质,不易导电;多数熔沸点较低;多数易燃烧,易分解才能正确解答此题.

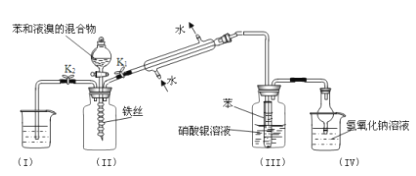
【题目】硫的化合物是常用的化工原料,但也是大气的主要污染物。综合治理其污染是环境化学当前的重要研究内容之一。
(1)一定温度下,将NH4HS固体放入定容真空容器中,可部分分解为硫化氢和氨气:NH4HS(s)![]() H2S(g)+NH3(g)
H2S(g)+NH3(g)
①可以判断上述分解反应已经达到化学平衡的是_____________(选填字母)
A. ![]() B.密闭容器中总压强不变
B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变 D.密闭容器中氨气的体积分数不变
②当上述反应达平衡时:p(NH3)×p(H2S)=a(Pa2),则平衡时容器中的总压为_______________Pa(用含a的代数式表示);(p(NH3)、p(H2S)分别代表NH3、H2S的压强,Pa为压强的单位)
③实验测得不同温度下的平衡数据列于下表:
温度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
平衡气体总浓度(×10-3mol/L) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
④NH4HS分解反应的焓变△H_________0(填“>”、“=”或“<”)
下图是上述反应过程中生成物浓度随时间变化的示意图。若t2时增大氨气的浓度且在t3时反应再次达到平衡,请在图上画出t2时刻后硫化氢、氨气的浓度随时间的变化曲线.(要有必要标注)____________

(2)一定温度下,反应2SO2+O2![]() 2SO3,达到平衡时,n(SO2):n(O2):n(SO3)=2:3:4。缩小体积,反应再次达到平衡时,n(O2)=0.8mol,n(SO3)=1.4mol,此时SO2的物质的量应是____________。
2SO3,达到平衡时,n(SO2):n(O2):n(SO3)=2:3:4。缩小体积,反应再次达到平衡时,n(O2)=0.8mol,n(SO3)=1.4mol,此时SO2的物质的量应是____________。
(3)25℃,吸收液Na2SO3溶液在吸收SO2的过程中,pH随n(SO3- ):n(HSO3﹣)变化关系如下表:
n(SO32﹣):n(HSO3﹣) | 91:9 | 1:1 | 1:91 |
pH | 8.2 | 7.2 | 6.2 |
①当吸收液呈中性时,溶液中离子浓度关系正确的是:______(选填字母)
A.c(Na+)=2c(SO32- )+c(HSO3-)
B.c(Na+)> c(HSO3-)> c(SO32- )>c(H+)=c(OH-)
C.c(Na+)+c(H+)= c(SO32- )+ c(HSO3-)+c(OH-)
②当吸收液的pH降至约为6时,需送至电解槽再生。再生示意图如下,请写出HSO3- 在阳极放电的电极反应式是___________________。

(4)已知:CH4(g)+2O2(g) = CO2 (g) +2H2O (l) △H= - Q1 kJ/mol
2H2(g)+O2(g) = 2H2 O (g) △ H= - Q2 kJ/mol
2H2(g)+O2(g) =2H2 O (l) △ H= - Q3 kJ/mol,
常温下,取体积比4:1的甲烷和氢气的混合气体11.2L(标况),经完全燃烧恢复常温,放出的热为_______________________。