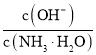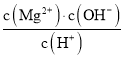题目内容
【题目】下列离子方程式或化学反应方程式与所述事实相符且正确的是
A.将![]() 气体通入一密闭容器中,达平衡后吸收QkJ热量,则该反应的热化学方程式为:
气体通入一密闭容器中,达平衡后吸收QkJ热量,则该反应的热化学方程式为:![]()
B.将少量![]() 气体通入NaClO溶液中:
气体通入NaClO溶液中:![]()
C.![]() 溶液中加入
溶液中加入![]() 溶液使
溶液使![]() 完全沉淀:
完全沉淀:![]()
D.向含有![]() 的溶液中通入
的溶液中通入![]() 充分反应:
充分反应:![]()
【答案】D
【解析】
A.SO3分解反应是可逆反应:![]() ,
,![]() 不可能完全反应,则该反应的热化学方程式为
不可能完全反应,则该反应的热化学方程式为![]() ,故A错误;
,故A错误;
B.将少量![]() 气体通入NaClO溶液中,发生的是氧化还原反应,离子反应为
气体通入NaClO溶液中,发生的是氧化还原反应,离子反应为![]() ,故B错误;
,故B错误;
C.![]() 溶液中加入
溶液中加入![]() 溶液使
溶液使![]() 完全沉淀的离子反应为
完全沉淀的离子反应为![]() ,故C错误;
,故C错误;
D.向含有![]() 的溶液中通入
的溶液中通入![]() ,由于Fe2+的还原性强于Br-,所以氯气先和Fe2+反应,剩余的氯气再氧化Br-,反应的离子方程式为
,由于Fe2+的还原性强于Br-,所以氯气先和Fe2+反应,剩余的氯气再氧化Br-,反应的离子方程式为![]() ,故D正确;
,故D正确;
答案:D。

练习册系列答案
 一本好题口算题卡系列答案
一本好题口算题卡系列答案
相关题目