题目内容
【题目】下列判断正确的是( )
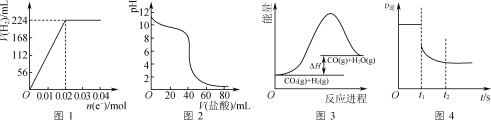
A.图1可表示电解200 mL 0.1 mol·L-1 NaCl溶液过程中,产生氢气体积(标准状况)与转移电子物质的量的关系曲线
B.图2可表示常温下0.1 mol·L-1盐酸滴加到40 mL 0.1 mol·L-1 NaOH溶液的滴定曲线
C.高温下能自发进行的反应CO2(g)+H2(g)![]() CO(g)+H2O(g)的能量变化如图3所示,则该反应的ΔS>0
CO(g)+H2O(g)的能量变化如图3所示,则该反应的ΔS>0
D.图4可表示反应N2(g)+3H2(g)![]() 2NH3(g)在t1时刻扩大容器体积时,v逆随时间的变化曲线
2NH3(g)在t1时刻扩大容器体积时,v逆随时间的变化曲线
【答案】CD
【解析】
A.电解NaCl溶液时,阴极始终是水电离生成的H+被还原为H2,因此氢气的体积随着转移电子的物质的量在不断增加,A项错误;
B.常温下0.1mol/L的NaOH溶液其pH是13,因此,滴定曲线中V(盐酸)=0mL即未滴加盐酸时,溶液的pH应为13,B项错误;
C.由图可知,该反应的![]() ,该反应能在高温下自发进行,根据
,该反应能在高温下自发进行,根据![]() 可知,该反应的
可知,该反应的![]() ,C项正确;
,C项正确;
D.t1时刻扩大容器体积,相当于降低体系的压强,因此t1时刻v逆会因为压强降低而减小;根据该反应的方程式可知,降低压强会使反应平衡逆向移动,NH3的量会逐渐下降,因此v逆会进一步减小直至达到新的平衡状态,D项正确;
答案选CD。

【题目】室温下进行下列实验,根据实验操作和现象所得到的结论正确的是( )
选项 | 实验操作和现象 | 结论 |
A | 向蛋白质溶液中加入醋酸铅溶液,产生白色沉淀 | 蛋白质发生了盐析 |
B | SO2通入Ba(NO3)2溶液中,产生白色沉淀 | 沉淀为BaSO3 |
C | 向蔗糖中加入适量浓硫酸并搅拌,蔗糖变黑,体积膨胀,并放出刺激性气味的气体 | 浓硫酸具有脱水性和强氧化性 |
D | 分别向等物质的量浓度的苯酚钠溶液和碳酸钠溶液中滴加酚酞,后者红色更深 | 碳酸酸性强于苯酚 |
A.AB.BC.CD.D