题目内容
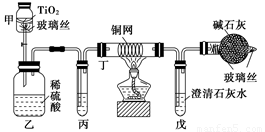
环境保护是我国的一项基本国策。含CN-的污水毒性极大,治理CN-的污水的方法之一是:在催化剂TiO2作用下,用NaClO将CN-氧化成CNO-,CNO-在酸性条件下继续被NaClO氧化成CO2、N2和H2O以及Cl-,其离子方程式为:CN-+ClO-====CNO-+Cl-;2CNO-+3ClO-+2H+====N2↑+2CO2↑+H2O+Cl-。某研究性学习小组用图15-6装置进行模拟实验,以证明上述处理CN-污水的有效性,并测定CN-被处理的百分率,下述实验装置是通过测定CO2的量来确定CN-处理的效果。
试根据要求完成下列问题:

图15-6
(1)将浓缩后含有CN-的污水(其中CN-浓度为0.05 mol·L-1)200 mL倒入甲装置中,再向甲装置中加入过量的漂白粉溶液,塞上橡皮塞,一段时间后,打开活塞,使溶液全部进入乙中,关闭活塞。
①乙装置中生成的气体除含有CO2、N2、HCl外还有副反应生成的Cl2等,写出生成Cl2的副反应的离子方程式:_____________________________________________________________。
②丙中加入的除杂试剂是__________。
A.饱和食盐水 B.饱和碳酸氢钠溶液
C.浓NaOH溶液 D.浓硫酸
③丁装置在实验中的作用是_______________。
④戊中盛有足量石灰水,若实验后戊中盛有足量石灰水,若实验后戊中共生成0.8 g沉淀,则该实验中CN-被处理的百分率为___________。
(2)上述实验中造成戊中碳酸钙质量测定值偏小的可能原因有(写出两点即可):________
_________________________________________________________。
(3)若有人想用测定氮气的量来确定CN-被处理的百分率,是否可行?如可行,还需要添加的仪器有________________________橡皮塞、导管及橡皮管。装置还可如何优化?
解析:本题是提供新信息、新情景试题,弄清反应:CN-+ClO-====CNO-+Cl-在甲中完成,反应:2CNO-+3ClO-+2H+====N2↑+2CO2↑+H2O+Cl-及Cl-+ClO-+2H+====Cl2↑+H2O在乙中完成,欲测定生成CO2的质量,丙、丁为除杂装置,丙中只能用食盐水来除HCl,碳酸氢钠会造成偏大误差,选其他碱性试剂会使CO2被部分或全部吸收,若要用测定的量只能用量气装置来测定氮气的体积,此时装置可利用碱液除去Cl2和HCl,只要在丙中加氢氧化钠溶液,戊中加石灰水,就可达到目的。
答案:(1)①Cl-+ClO-+2H+====Cl2↑+H2O
②A ③除去混合气体中的Cl2 ④80%
(2)装置乙、丙、丁中残留CO2;反应速率较快,一部分CO2从戊中逸出
(3)广口瓶、量筒 省去丁装置,只要在丙中加氢氧化钠溶液,戊中加石灰水