题目内容
16.下列说法中,错误的是( )| A. | 天然气的主要成分是CH4 | |
| B. | 酸性:乙酸>碳酸>次氯酸 | |
| C. | 淀粉、纤维素、蚕丝、油脂都是高分子化合物 | |
| D. | 石油的分馏产品如汽油、煤油、柴油等都是混合物 |
分析 A.天然气的主要成分是甲烷;
B.根据强酸制弱酸的原理分析;
C.高分子化合物的相对分子质量一般达1万以上、一般具有重复结构单元;
D.纯净物是单一的一种物质.
解答 解:A.甲烷是天然气的主要成分,故A正确;
B.根据强酸制弱酸的原理,乙酸与碳酸钠反应能生成碳酸,所以乙酸酸性比碳酸强;碳酸与次氯酸钙反应能生成次氯酸,所以碳酸酸性比次氯酸强,所以酸性强弱:乙酸>碳酸>次氯酸,故B正确;
C.油脂相对分子质量较小,不是高分子化合物,故C错误;
D.汽油、煤油、柴油是多种烃组成的混合物,故D正确.
故选C.
点评 本题考查天然气的成分、高分子化合物、酸性比较以及混合物等,题目难度不大,注意汽油、煤油、柴油是多种烃组成的混合物,注意规律的掌握理解.

练习册系列答案
 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案
相关题目
6.如图所示的某有机反应,其反应类型为( )
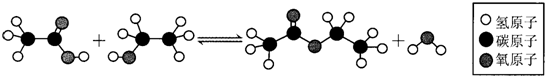

| A. | 取代反应 | B. | 加成反应 | C. | 水解反应 | D. | 氧化反应 |
7.研究反应物的化学计量数与产物之间的关系时,使用类似数轴的方法表示更便于理解.下列表达正确的是( )
| A. | Na2CO3溶液和盐酸反应后溶液中的钠盐: | |
| B. | NaOH溶液与CO2反应后溶液中的钠盐: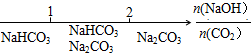 | |
| C. | Fe与稀硝酸反应的氧化产物: | |
| D. | AlCl3溶液中滴加氨水后铝元素的存在形式: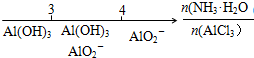 |
4.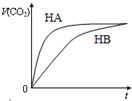 有等体积,浓度均为0.1mol/L的三种溶液:①HA溶液②HB溶液③NaHCO3溶液,已知将①、②分别与③混合,实验测得产生的CO2气体体积(v)随时间(t)变化的如图所示,下列说法正确的是( )
有等体积,浓度均为0.1mol/L的三种溶液:①HA溶液②HB溶液③NaHCO3溶液,已知将①、②分别与③混合,实验测得产生的CO2气体体积(v)随时间(t)变化的如图所示,下列说法正确的是( )
 有等体积,浓度均为0.1mol/L的三种溶液:①HA溶液②HB溶液③NaHCO3溶液,已知将①、②分别与③混合,实验测得产生的CO2气体体积(v)随时间(t)变化的如图所示,下列说法正确的是( )
有等体积,浓度均为0.1mol/L的三种溶液:①HA溶液②HB溶液③NaHCO3溶液,已知将①、②分别与③混合,实验测得产生的CO2气体体积(v)随时间(t)变化的如图所示,下列说法正确的是( )| A. | 物质酸性的比较:HB>HA>H2CO3 | |
| B. | 反应结束后所得两溶液中,c(B-)>c(A-) | |
| C. | 上述三种溶液中由水电离的c(OH-)大小:NaHCO3溶液>HB溶液>HA溶液 | |
| D. | HA溶液和NaHCO3溶液反应所得溶液中:c(A-)+c(HA)=0.10mol/L |
1.等质量的SO2和SO3相比较,下列判断正确的是( )①含有的氧原子个数之比为5:6;②含有的氧原子个数之比为6:5;③含有的硫原子个数之比为5:4;④含有的硫原子个数相等.
| A. | ①和③ | B. | ①和④ | C. | ②和④ | D. | ②和③ |
8.向下列溶液中滴加稀H2S04,一开始出现白色沉淀,继续滴加稀H2S04,沉淀又溶解的是( )
| A. | AlCl3 | B. | NaAl02 | C. | Mgcl2 | D. | BaCl2 |
4.研究氮的固定具有重要意义.
(1)雷雨天气中发生自然固氮后,氮元素转化为硝酸盐而存在于土壤中.处于研究阶段的化学固氮新方法是N2在催化剂表面与水发生如下反应:
2N2(g)+6H2O(l)=4NH3(g)+3O2(g)△H K ①
已知:N2(g)+3H2(g)=2NH3(g)△H1=-92.4kJ•mol-1 K1②
2H2(g)+O2(g)=2H2O(l)△H2=-571.6kJ•mol-1 K2③
则△H=+1530kJ•mol-1;K=$\frac{{{K}_{1}}^{2}}{{{K}_{2}}^{3}}$(用K1和 K2表示).
(2)在四个容积为2L的密闭容器中,分别充入1mol N2、3mol H2O,在催化剂条件下进行反应①3小时,实验数据见下表:
下列能说明反应①达到平衡状态的是bd(填字母).
a.NH3和O2的物质的量之比为4:3
b.反应混合物中各组份的质量分数不变
c.单位时间内每消耗1molN2的同时生成2molNH3
d.容器内气体密度不变
若第三组反应3h后已达平衡,第三组N2的转化率为3×10-4%;与前三组相比,第四组反应中NH3生成量最小的原因可能是催化剂在80℃活性减小,反应速率反而减慢.
(1)雷雨天气中发生自然固氮后,氮元素转化为硝酸盐而存在于土壤中.处于研究阶段的化学固氮新方法是N2在催化剂表面与水发生如下反应:
2N2(g)+6H2O(l)=4NH3(g)+3O2(g)△H K ①
已知:N2(g)+3H2(g)=2NH3(g)△H1=-92.4kJ•mol-1 K1②
2H2(g)+O2(g)=2H2O(l)△H2=-571.6kJ•mol-1 K2③
则△H=+1530kJ•mol-1;K=$\frac{{{K}_{1}}^{2}}{{{K}_{2}}^{3}}$(用K1和 K2表示).
(2)在四个容积为2L的密闭容器中,分别充入1mol N2、3mol H2O,在催化剂条件下进行反应①3小时,实验数据见下表:
| 序号 | 第一组 | 第二组 | 第三组 | 第四组 |
| t/℃ | 30 | 40 | 50 | 80 |
| NH3生成量/(10-6mol) | 4.8 | 5.9 | 6.0 | 2.0 |
a.NH3和O2的物质的量之比为4:3
b.反应混合物中各组份的质量分数不变
c.单位时间内每消耗1molN2的同时生成2molNH3
d.容器内气体密度不变
若第三组反应3h后已达平衡,第三组N2的转化率为3×10-4%;与前三组相比,第四组反应中NH3生成量最小的原因可能是催化剂在80℃活性减小,反应速率反而减慢.