题目内容
人造地球卫星用到的一种高能电池——银锌蓄电池,它在放电时的电极反应为:Zn + 2OH– –2e–=ZnO + H2O,Ag2O + H2O + 2e–=2Ag + 2OH–,下列叙述中,正确的是
| A.Ag2O 是负极,并被氧化 |
| B.电流由锌经外电路流向氧化银 |
| C.工作时,负极区溶液pH减小,正极区pH增大 |
| D.溶液中OH-向正极移动,K+、H+向负极移动 |
C
原电池负极锌失电子,发生氧化反应,电子经导线流向正极,Ag2O得电子,发生还原反应,而电流的方向和电子的流向正好相反。
由放电电极反应可知,负极消耗OH–,碱性减小,pH减小,而正极正好相反。
电解质溶液的阴离子一般向负极移动,阳离子一般向正极移动(或者说:负极由于消耗了OH—,故它向负极移动)
故答案为C
由放电电极反应可知,负极消耗OH–,碱性减小,pH减小,而正极正好相反。
电解质溶液的阴离子一般向负极移动,阳离子一般向正极移动(或者说:负极由于消耗了OH—,故它向负极移动)
故答案为C

练习册系列答案
相关题目
 3Zn(OH)2+2Fe(OH)3+4KOH,以下说法错误的是
3Zn(OH)2+2Fe(OH)3+4KOH,以下说法错误的是 ,则有关说法正确的是
,则有关说法正确的是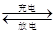 +V2++2H+。
+V2++2H+。