题目内容
(1)R+与S2–所含电子数相同,则R元素的原子序数为
(2)一种基于酸性燃料电池原理设计的酒精检测仪,正极上的反应为:O2 + 4e– + 4H+ = 2H2O,检测有酒精时,电解质溶液中的H+向 极移动,该电池负极上的反应为:
(3)X、Y、Z、M、G五种分属三个短周期主族元素,且原子序数依次增大。Z存在质量数为23,中子数为12的核素A;Y、M同主族,可形成MY2、MY3两种分子。
回答下列问题:
①用化学符号表示核素A: ;
②上述元素的最高价氧化物对应的水化物酸性最强的是 (写化学式),写出该物质与氢氧化钠溶液反应的离子方程式: ;
③X2M的电子式为 ;
④ZG用途广泛,下列说法正确的是: 。
| A.作调味剂 | B.用于食物防腐 | C.用于氯碱工业 | D.用于医疗 |
(1)19 (2)正 CH3CH2OH – 4e– + H2O = CH3COOH + 4H+
(3) ① ② HClO4 OH– + H+ = H2O
② HClO4 OH– + H+ = H2O
③ ④ ABCD
④ ABCD
解析试题分析:(1)S2–所含电子数为18,则R所含电子数为18+1=19,故其原子序数为19。
(2)理论上O2可把酒精氧化为CO2,但在酒精检测仪中氧气只能把酒精氧化到乙酸,原电池中阳离子向正极(带负电)移动,故负极的电极反应为:CH3CH2OH – 4e– + H2O = CH3COOH + 4H+
(3)X、Y、Z、M、G五种分属三个短周期主族元素,且原子序数依次增大,则X为氢元素;Z的核素A质量数为23,中子数为12,则质子数为11,所以M为钠元素;Y、M同主族,可形成MY2、MY3两种分子,则Y、M分别为氧和硫元素,MY2、MY3分别为SO2和SO3,G只能是氯元素。
①核素A的符号为: ;②上述五种元素中氯元素的非金属性最强,所以其最高价氧化物的水化物酸性最强,其化学式为:HClO4(高氯酸),高氯酸为强酸,与氢氧化钠溶液反应的离子方程式为:OH– + H+ = H2O;③X2M的电子式为H2S,其电子式见答案;④ZG是氯化钠,其用途广泛,可用作调味剂、食物防腐剂、氯碱工业的原料、用于医疗(生理盐水)等。
;②上述五种元素中氯元素的非金属性最强,所以其最高价氧化物的水化物酸性最强,其化学式为:HClO4(高氯酸),高氯酸为强酸,与氢氧化钠溶液反应的离子方程式为:OH– + H+ = H2O;③X2M的电子式为H2S,其电子式见答案;④ZG是氯化钠,其用途广泛,可用作调味剂、食物防腐剂、氯碱工业的原料、用于医疗(生理盐水)等。
考点:本题是元素推断、性质比较、化学用语、电极反应、物质用途、离子方程式等多方面知识的考查。

 全能练考卷系列答案
全能练考卷系列答案 一课一练课时达标系列答案
一课一练课时达标系列答案根据下列五种元素的第一至第四电离能数据(单位: kJ·mol-1),回答下列各题:
| 元素代号 | I1 | I2 | I3 | I4 |
| Q | 2 080 | 4 000 | 6 100 | 9 400 |
| R | 496 | 4 562 | 6 912 | 9 543 |
| S | 738 | 1 451 | 7 733 | 10 540 |
| T | 578 | 1 817 | 2 745 | 11 575 |
| U | 420 | 3 100 | 4 400 | 5 900 |
(1)在周期表中,最可能处于同一族的是________。
A.Q和R B.S和T C.T和U D.R和T E.R和U
(2)下列离子的氧化性最弱的是________。
A.S2+ B.R2+ C.T3+ D.U+
(3)下列元素中,化学性质和物理性质最像Q元素的是____。
A.硼 B.铍 C.氦 D.氢
(4)每种元素都出现相邻两个电离能的数据相差较大的情况,这一事实从一个侧面说明:______,如果U元素是短周期元素,你估计它的第2次电离能飞跃数据将发生在失去第_____个电子时。
(5)如果R、S、T是同周期的三种主族元素,则它们的原子序数由小到大的顺序是________,其中元素________的第一电离能异常高的原因是__________________。
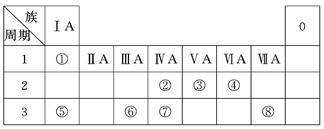
下图是元素周期表的一部分,其中每个数字编号代表对应的一种元素。
| ① | | | ||||||
| | | | | ② | ③ | ④ | | |
| ⑤ | | ⑥ | ⑦ | | | ⑧ | ⑨ | |
请按要求回答下列问题:
(1)画出元素②的原子结构示意图 。
(2)属于稀有气体的元素编号是_______,可作半导体材料的元素编号是______。
(3)③、⑦两种元素相比较,非金属性强的是 (填元素符号)。
(4)元素④的单质与元素⑤的单质反应可生成两种化合物,化学式分别是 , 。
(5)元素③和元素⑧的氢化物均极易溶于水,用两根玻璃棒分别蘸取它们的浓溶液,相互接近时,可
看到大量的白烟,写出产生该现象的化学方程式: 。
 Si(s)+2CO(g)
Si(s)+2CO(g) SiHCl3(l)+H2(g) + Q(Q>0)
SiHCl3(l)+H2(g) + Q(Q>0) Si(纯)+3HCl(g)
Si(纯)+3HCl(g)