题目内容
对可逆反应 4N3(g )+5O2 ( g)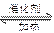 4NO(g)+ 6H2O ( g ) ,下列叙述正确的是
4NO(g)+ 6H2O ( g ) ,下列叙述正确的是
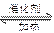 4NO(g)+ 6H2O ( g ) ,下列叙述正确的是
4NO(g)+ 6H2O ( g ) ,下列叙述正确的是| A.反应达到平衡时,若两种反应物的转化率相等,则起始投入的 n (NH3 ) : n (O 2 ) =" 4:5" |
| B.反应达到平衡后,对体系一直进行加压,平衡总是向逆向移动 |
| C.反应达到平衡时,若向压强固定的密闭容器中充入稀有气体,平衡不移动 |
| D.当v正(NH3 ) : v正(NO)=" l" : 1 时,说明该化学反应已经达到平衡 |
A
平衡时,反应物的转化率相等,则起始投人量之比应该等于化学计量数之比,故 A 正确;当加压到一定压强时,气态水变为非气态,平衡会向正向移动,故 B 也错;充入稀有气体而压强不变,相当于增大容积,平衡向体积增大方向移动,C 错; NH3、NO的正反应速率都是向右方向的速率,平衡与否其反应速率之比都等于化学计量数之比,故 D 错。选A 。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 2C(g),达平衡时,在相同温度下测得容器内混合气体的压强是反应前的
2C(g),达平衡时,在相同温度下测得容器内混合气体的压强是反应前的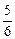 ,则A的转化率为
,则A的转化率为 Fe3O4(s)+ 4H2(g),反应的化学平衡常数的表达式为( )
Fe3O4(s)+ 4H2(g),反应的化学平衡常数的表达式为( )




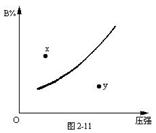 ①m+n>P;②x点表示该反应的正反应速率大于逆反应速率;③n>p;④x点比y点时的反应速率慢。
①m+n>P;②x点表示该反应的正反应速率大于逆反应速率;③n>p;④x点比y点时的反应速率慢。