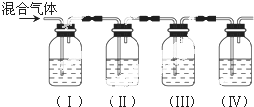
题目内容
16.下列离子方程式中正确的是( )| A. | 向碳酸钠溶液中加入足量的盐酸 CO32-+2H+═CO2↑+H2O | |
| B. | 单质铁和三氯化铁溶液反应生成氯化亚铁 Fe+Fe3+═2Fe2+ | |
| C. | 金属钠与水反应生成氢氧化钠和氢气Na+H2O═Na++OH-+H2↑ | |
| D. | 氯化铵晶体和石灰粉共热产生氨气 NH4++OH-═NH3↑+H2O |
分析 A.向碳酸钠溶液中加入足量的盐酸,生成二氧化碳和水;
B.电荷不守恒;
C.质量不守恒;
D.为固体之间的反应,不写成离子方程式.
解答 解:A.向碳酸钠溶液中加入足量的盐酸,生成二氧化碳和水,反应的离子方程式为 CO32-+2H+═CO2↑+H2O,故A正确;
B.单质铁和三氯化铁溶液反应生成氯化亚铁,反应的离子方程式应为Fe+2Fe3+═3Fe2+,故B错误;
C.金属钠与水反应生成氢氧化钠和氢气2Na+2H2O═2Na++2OH-+H2↑,故C错误;
D.为固体之间的反应,不写成离子方程式,故D错误.
故选A.
点评 本题考查离子反应的书写,为高考高频考点,把握发生的化学反应为解答的关键,注意单质、弱电解质、沉淀等在离子反应中保留化学式,注重基础知识的考查,易错点为D,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.下列关于乙酸的说法正确的是( )
| A. | 乙酸能够使紫色石蕊试剂变红,所以乙酸是强酸 | |
| B. | 食醋除去水垢的现象证明了酸性:乙酸>碳酸 | |
| C. | 乙酸与乙醇发生的酯化反应不属于取代反应 | |
| D. | 在制备乙酸乙酯的实验中,用18O标记乙醇,在产物乙酸乙酯中检测不到18O |
7.下列说法正确的是( )
| A. | 萘(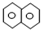 )是最简单的稠环芳香烃,萘与足量氢气充分加成的产物一氯代物有2种 )是最简单的稠环芳香烃,萘与足量氢气充分加成的产物一氯代物有2种 | |
| B. | 酚酞的结构如图所示,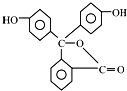 其结构中含有羟基(-OH),故酚酞属于醇 其结构中含有羟基(-OH),故酚酞属于醇 | |
| C. | 溴水能将甲苯、己烯、CCl4、乙醇四种溶液鉴别开来 | |
| D. | 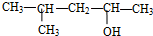 的名称为2-甲基-4-戊醇 的名称为2-甲基-4-戊醇 |
4.过氧化氢是重要的氧化剂、还原剂,它的水溶液又称为双氧水,常用作消毒、杀菌、漂白等.某化学兴趣小组取一定量的过氧化氢溶液,准确测定了过氧化氢的含量,并探究了过氧化氢的性质.
Ⅰ.测定过氧化氢的含量
步骤如下并填写下列空白:
(1)将10.00mL密度为ρ g/mL的过氧化氢溶液稀释至250mL.量取稀释后的过氧化氢溶液25.00mL至锥形瓶中,加入稀硫酸酸化,作被测试样.此过程中需要用到的定量仪器250ml容量瓶,滴定管或移液管.
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下,请完成该反应方程
2MnO4-+5H2O2+6H+→2Mn2++8H2O+502
(3)滴定时,将高锰酸钾标准溶液注入滴定管中,滴定到达终点的现象是滴入最后一滴高锰酸钾溶液,溶液呈紫红色,且30秒内不褪色
(4)重复滴定二次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为$\frac{0.085cV}{ρ}$.
(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果偏高(填“偏高”“偏低”“不变”).
Ⅱ.探究过氧化氢的性质
该化学小组根据所提供的实验条件设计了两个实验,分别证明了过氧化氢的氧化性和不稳定性.(实验条件:试剂只有过氧化氢溶液、氯水、淀粉碘化钾溶液、二氧化锰,实验仪器及用品可自选.)
请将他们所选的实验试剂和实验现象填入下表:
Ⅰ.测定过氧化氢的含量
步骤如下并填写下列空白:
(1)将10.00mL密度为ρ g/mL的过氧化氢溶液稀释至250mL.量取稀释后的过氧化氢溶液25.00mL至锥形瓶中,加入稀硫酸酸化,作被测试样.此过程中需要用到的定量仪器250ml容量瓶,滴定管或移液管.
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下,请完成该反应方程
2MnO4-+5H2O2+6H+→2Mn2++8H2O+502
(3)滴定时,将高锰酸钾标准溶液注入滴定管中,滴定到达终点的现象是滴入最后一滴高锰酸钾溶液,溶液呈紫红色,且30秒内不褪色
(4)重复滴定二次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为$\frac{0.085cV}{ρ}$.
(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果偏高(填“偏高”“偏低”“不变”).
Ⅱ.探究过氧化氢的性质
该化学小组根据所提供的实验条件设计了两个实验,分别证明了过氧化氢的氧化性和不稳定性.(实验条件:试剂只有过氧化氢溶液、氯水、淀粉碘化钾溶液、二氧化锰,实验仪器及用品可自选.)
请将他们所选的实验试剂和实验现象填入下表:
| 实 验 内 容 | 实 验 试 剂 | 实 验 现 象 |
| 探究氧化性 | 取适量碘化钾淀粉溶液于试管中,加入过氧化氢溶液 | 溶液变蓝色 |
| 探究不稳定性 | 取适量过氧化氢溶液于试管中,加热, 用带火星的木条检验 | 产生气泡,木条复燃 |
1.石蕊是一种弱酸,石蕊分子(HZ)及其酸根离子(Z-)在水溶液中具有完全不同的颜色.其中HZ的颜色是( )
| A. | 红色 | B. | 紫色 | ||
| C. | 蓝色 | D. | 视溶液的酸碱性待定H2 |
8.下列物质发生变化时,所克服的粒子间的相互作用属同种类型的是( )
| A. | 液态HF与液态HBr分别受热变为气体 | |
| B. | 氯化铵与苯分别受热变为气体 | |
| C. | 氯化钠与氯化氢分别溶解在水中 | |
| D. | 碘与干冰分别受热变为气体 |
5.NM-3是处于临床试验阶段的小分子抗癌药物,分子结构如图所示,下列说法正确的是( )

| A. | 该有机物的分子式为C12H12O6 | |
| B. | 该有机物的分子中只含有1个手性碳原子 | |
| C. | 可用FeCl3溶液检验该有机物质中是否含有苯酚 | |
| D. | 1mol该有机物最多可以和4molNaOH反应 |
6.某烷烃的结构简式是CH3CH2CH2CH(CH2CH3)CH3,它的正确命名是( )
| A. | 3-甲基己烷 | B. | 4-乙基戊烷 | C. | 2-乙基戊烷 | D. | 2,2-二甲基戊烷 |