题目内容
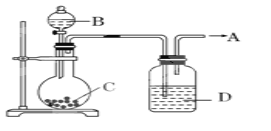
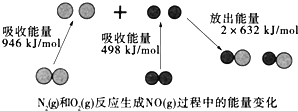
【题目】化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的.如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化,下列说法错误的是
A.该反应的热化学方程式为:N2(g)+O2(g)═2NO(g)△H=+180kJmol﹣1
B.1mol N2(l)和NA个O2(l)反应生成2mol NO(g)时,吸收的能量为180kJ
C.1mol N2(g)和1mol O2(g)具有的总能量小于2mol NO(g)具有的总能量
D.通常情况下,N2(g)和O2(g)混合不能直接生成NO(g)
【答案】B
【解析】A、△H=反应物断裂化学键吸收的能量﹣生成物形成化学键放出的能量,N2(g)+O2(g)═2NO(g),△H=946KJ/mol+498KJ/mol﹣2×632KJ/mol=+180kJ/mol,故A正确;
B、由A可知,1mol N2(g)和NA个O2(g)反应生成2mol NO(g)时,吸收的能量为180kJ,故B错误;
C、N2(g)+O2(g)═2NO(g),△H=+180kJ/mol,为吸热反应,所以1mol N2(g)和1mol O2(g)具有的总能量小于2mol NO(g)具有的总能量,故C正确;
D、通常情况下,N2(g)和O2(g)不能发生化学反应,故D正确;
故选B.

 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案【题目】镁的单质及其化合物用途非常广泛。
(1)镁热还原法可制备铷、钛等金属,已知下列物理常数:
Mg | Rb | RbCl | MgCl2 | |
熔点/℃ | 648 | 38.89 | 718 | 714 |
沸点/℃ | 1107 | 688 | 1390 | 1412 |
在750℃时可实现用镁还原RbCl制Rb,该反应能够发生的原因是_________________________________(用文字和化学方程式说明)。
(2)无机抗菌剂Mg2ClO(OH)3·H2O(碱式次氯酸镁)可由MgCl2、NaOH及Cl2反应制得,该反应的化学方程式为______________________________________。
(3)CaC2冶镁的原理为CaC2(s)+MgO(s)![]() CaO(s)+Mg(g)+2C(s) △H,反应达到平衡时Mg的产率随温度的变化如图所示。
CaO(s)+Mg(g)+2C(s) △H,反应达到平衡时Mg的产率随温度的变化如图所示。

①△H__________(填“>"或“<”,下同)0。
②已知A、B中固体总质量相等,则![]() :A__________B。
:A__________B。
(4)Mg(OH)2浆液可脱除烟气中的SO2,其脱硫效率、pH及时间的关系如图所示。

Mg(OH)2浆液脱除SO2的过程中包含的主要反应如下:
Ⅰ.Mg(OH)2+SO2=MgSO3+H2O
Ⅱ.MgSO3+SO2+H2O=Mg(HSO3)2
Ⅲ.Mg(HSO3)2+Mg(OH)2=2MgSO3+2H2O
Ⅳ.2MgSO3+O2=2MgSO4
已知:20℃时,H2SO3的电离平衡常数K1=1.54×10-2、K2=1.02×10-7;25℃时,Ksp[Mg(OH)2]=1.2×10-11,MgSO3,的溶解度为0.646g。
①脱硫过程中使浆液pH减小最显著的反应是__________(填“Ⅰ”“Ⅱ”“Ⅲ”或“Ⅳ”)。
②约900s之后,脱硫效率明显降低,其原因是________________________。